题目内容
实验室中取氯酸钾和二氧化锰的混合物15.5克,加热制取氧气。待充分反应后,冷却,称得固体残渣的质量为10.7克。为了节约药品,将固体残渣放入55克蒸馏水中,充分溶解后过滤,回收二氧化锰和滤液。计算:
(1)回收得到二氧化锰的质量。
(2)滤液中溶质的质量分数(结果精确到0.01)。
解:由题意知,生成氧气的质量为15.5克-10.7克=4.8克……………………………
设反应中生成KCl的质量为x。
2KClO3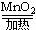 2KCl + 3O2↑
2KCl + 3O2↑
2×74.5 3×32
x 4.8克
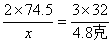
x=2×74.5×4.8克/3×32=7.45克…………………………………
MnO2的质量为:10.7-7.45克=3.25克
KCl溶液中溶质的质量分数为:7.45克/(7.45克+55克)=0.12(即12%)…
答:回收得到MnO2的质量为3.25克,滤液中溶质的质量分数为0.12(即12%)

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
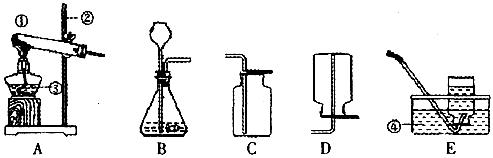
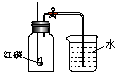 冷却至室温,试回答:(1)红磷在广口瓶内未能全
冷却至室温,试回答:(1)红磷在广口瓶内未能全 FeSO4 (B)CaCO3
FeSO4 (B)CaCO3