题目内容
20.某兴趣小组利用以下实验装置模拟工业炼铁的主要过程: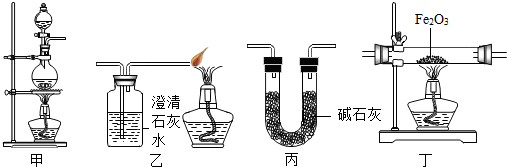
(1)装置甲中发生的反应为:HCOOH ( 甲酸 )$\frac{\underline{\;浓硫酸\;}}{加热}$ CO↑+H2O.
(2)请按合适的顺序连接好以下装置:甲→丙→丁→乙.
(3)丙装置中碱石灰(氧化钙与氢氧化钠混合物)的作用是除去CO中的水蒸气.
(4)丁装置中反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe.
(5)为了探究影响反应产物的外界因素,在Fe2O3与CO反应部位,该小组同学分别用酒精灯和酒精喷灯进行了两次实验,结果如下:
| 加热方式 | 通CO加热时间/min | 澄清石灰水变 浑浊时间/min | 产物颜色 | 产物能否全部 被磁铁吸引 |
| 酒精灯 | 30 | 5 | 黑色 | 能 |
| 酒精喷灯 | 30 | 1 | 黑色 | 能 |
②丙同学查找资料发现,Fe3O4也能被磁铁吸引,对黑色产物成分提出以下三种假
设:i.全部为铁;ii.全部为四氧化三铁;iii.四氧化三铁和铁的混合物.
③通过进一步定量实验,黑色产物所含元素组成和质量分数如下:
| 样品序号 | 加热方式 | 元素组成和质量分数 |
| 产物样品Ⅰ | 酒精灯 | w(Fe)=74.4%、w(O)=25.6% |
| 产物样品Ⅱ | 酒精喷灯 | w(Fe)=100% |
分析 (2)根据制备CO,除杂、还原氧化铁、尾气处理连接装置;
(3)丙装置中碱石灰的作用是除杂;
(4)在高温的条件下,一氧化碳还原氧化铁;
(5)①因为产物能全部被磁铁吸引,所以不会有碳生成,又因为CO作还原剂化合价升高不可能生成碳单质,据此分析;②根据Fe3O4也能被磁铁吸引,则组合可能为全部为铁,全部为Fe3O4,铁和Fe3O4都有;③设总质量为1g,则铁的质量为x,Fe3O4为(1-x),根据铁的含量列方程求解.
解答 解:(2)根据实验原理,应分为制备CO,除杂、还原氧化铁、尾气处理连接装置,所以顺序为甲丙丁乙,故答案为:丙;丁;乙;
(3)丙装置中碱石灰的作用是除杂,所以作用为除去CO中的水蒸气,故答案为:除去CO中的水蒸气;
(4)在高温的条件下,一氧化碳与氧化铁反应生成铁和二氧化碳;故填:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe;
(5)①因为产物能全部被磁铁吸引,所以不会有碳生成,又因为CO作还原剂化合价升高不可能生成碳单质,故答案为:碳单质不会被磁铁吸引;CO作还原剂化合价升高不可能生成碳单质;
②根据四氧化三铁也能被磁铁吸引,则组合可能为全部为铁,全部为四氧化三铁,铁和四氧化三铁都有,故答案为:全部为四氧化三铁;四氧化三铁和铁的混合物;
③设总质量为1g,则铁的质量为x,四氧化三铁的质量为(1-x),又氧的含量为25.6%,所以有$\frac{(1-x)×\frac{64}{232}}{1}$=25.6%,解得x=0.0720,所以铁的含量为7.20%,四氧化三铁的含量为1-7.20%=92.8%;故答案为:w(Fe3O4)=92.8%、w(Fe)=7.2%.
点评 本题考查了气体的制备及其工业炼铁的装置的选择等,题目涉及的知识点较多,侧重于基础知识的综合应用的考查,题目难度中等.

| A. | 硫酸铜、氯化镁、氢氧化钠、氯化钠 | B. | 硫酸铜、氢氧化钠、氯化镁、氯化钠 | ||
| C. | 硫酸铜、氯化镁、氯化钠、氢氧化钠 | D. | 氢氧化钠、硫酸铜、氯化镁、氯化钠 |
| A. | 分子、原子、离子都是构成物质的微粒 | |
| B. | 物质在水中的溶解过程实质上是原子重新组合的过程 | |
| C. | 化学变化的过程实质上是原子重新组合的过程 | |
| D. | 水的三态变化中,分子的能量、运动速率不变 |
| A. | 水是由氢分子和氧原子构成的 | |
| B. | 水是由氢、氧两种元素组成的 | |
| C. | 水分子是由两个氢分子和一个氧原子构成的 | |
| D. | 一个水分子是由氢原子和氧原子构成的 |
 如图所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b.请回答:
如图所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b.请回答: