题目内容
3.某同学为了测定一瓶失去标签的NaOH溶液的溶质质量分数,取80gFeCl3溶液,向其中逐滴加入待测的NaOH溶液,至不再产生沉淀共用去200gNaOH溶液,过滤后得滤液质量为173g,请计算下列问题.(温馨提示:FeCl3+3NaOH═Fe(OH)3↓+3NaCl)
(1)求反应后生成沉淀的质量为107g.
(2)求待测溶液的溶质质量分数.
分析 (1)根据质量守恒定律计算生成沉淀的质量;
(2)根据沉淀的质量计算参加反应的氢氧化钠的质量,然后计算质量分数.
解答 解:(1)生成沉淀的质量为:80g+200g-173g=107g;
(2)设参加反应的氢氧化钠的质量为x
FeCl3+3NaOH═Fe(OH)3↓+3NaCl
120 107
x 107g
$\frac{120}{x}$=$\frac{107}{107g}$
x=120g
待测溶液的质量分数为:$\frac{120g}{200g}$×100%=60%.
故答案为:(1)107;
(2)待测溶液的溶质质量分数是60%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
相关题目
14.如图是利用海水提取粗盐的过程,下列说法中错误的是( )
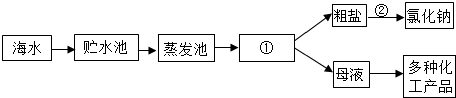

| A. | 图中①是结晶池 | |
| B. | 图中②的操作过程是溶解、过滤、结晶 | |
| C. | 析出晶体后的母液是氯化钠的饱和溶液 | |
| D. | 蒸发池是利用氯化钠的溶解度受温度影响变化大的原理 |
8.计算题
(1)常温下,要将质量分数为10%的氯化钠溶液100g变为质量分数为20%的氯化钠,常用的方法有加入溶质和蒸发溶剂.请通过计算回答:①需要加入氯化钠晶体12.5 g. ②需要蒸发掉50g水.
(2)一包氯化镁和硫酸钠组成的混合物中,为测定其中氯化镁的质量分数,小亮同学称取该混合物样品20g,完全溶于水中,然后取用了一定溶质质量分数的氢氧化钠溶液100g,平均分四次加入其中,充分振荡后,测得实验数据如下表所示,请分析并进行相关的计算:
①表中X的数值是5.8;
②试求原固体混合物样品中氯化镁的质量分数是71.25%.
(1)常温下,要将质量分数为10%的氯化钠溶液100g变为质量分数为20%的氯化钠,常用的方法有加入溶质和蒸发溶剂.请通过计算回答:①需要加入氯化钠晶体12.5 g. ②需要蒸发掉50g水.
(2)一包氯化镁和硫酸钠组成的混合物中,为测定其中氯化镁的质量分数,小亮同学称取该混合物样品20g,完全溶于水中,然后取用了一定溶质质量分数的氢氧化钠溶液100g,平均分四次加入其中,充分振荡后,测得实验数据如下表所示,请分析并进行相关的计算:
| 次数 | 1 | 2 | 3 | 4 |
| 加入氢氧化钠溶液的质量(g) | 25 | 25 | 25 | 25 |
| 生成沉淀的质量(g) | 2.9 | X | 8.7 | 8.7 |
②试求原固体混合物样品中氯化镁的质量分数是71.25%.
6.区别下列各组物质,所选择的试剂或方法错误的是( )
| A. | 硬水和软水--肥皂水 | B. | 银单质和锌单质--硝酸镁溶液 | ||
| C. | 空气和氧气--带火星的木条 | D. | H2O和H2O2溶液--二氧化锰 |
 眼镜是人们常用的护眼工具,如图所示是一款变色眼镜的示意图:
眼镜是人们常用的护眼工具,如图所示是一款变色眼镜的示意图: