题目内容
(本题共6分)硫化氢气体是一种大气污染物,它在空气中点燃完全燃烧时,生成二氧化硫和水,把硫化氢气体通入浓硫酸中,发生的反应为H2S+H2SO4(浓)== SO2+X↓+2H2O
(1)写出硫化氢气体在空气中燃烧的化学方程式 ;
(2)硫化氢与浓硫酸反应过程中,下列哪些量保持不变: ;(请选择字母编号填空)
A.原子种类
B.分子种类
C.原子个数
D.分子个数
E.所有元素化合价
F.元素的种类
(3)若尾气中含有硫化氢气体,小明经过认真分析,认为不能用浓硫酸来吸收硫化氢气体,请问小明的理由是: 。
(1)2H2S+3O2点燃2H2O+2SO2 (2)ACF
(3)浓H2SO4与H2S反应会产生SO2,SO2会造成环境污染
【解析】
试题分析:(1)硫化氢气体是在空气中点燃完全燃烧时,生成二氧化硫和水,化学方程式:2H2S+3O2点燃2H2O+2SO2
(2)根据质量守恒定律:化学反应前后:原子种类、原子个数、元素的种类都不变,而分子种类一定变,分子个数、元素化合价都是可能变,故硫化氢与浓硫酸反应过程中,保持不变量选ACF
(3)根据把硫化氢气体通入浓硫酸中,发生的反应为H2S+H2SO4(浓)== SO2+X↓+2H2O,故不能用浓硫酸来吸收硫化氢气体,原因是:浓H2SO4与H2S反应会产生SO2,SO2会造成环境污染
考点:化学方程式的书写,质量守恒定律,大气的污染物

 名校课堂系列答案
名校课堂系列答案(10分)某化学兴趣小组回收利用废旧干电池。
实验1:回收填料中的二氧化锰和氯化铵
查阅资料:废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水。兴趣小组的同学们设计回收物质的流程如图所示。
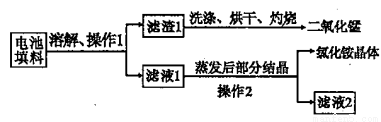
(1)操作1和操作2的名称都是_______,该操作中玻璃棒的作用是_______________。
(2)灼烧滤渣l的目的是________________________ 。
实验2:利用外壳回收物锌制取氢气及相关探究
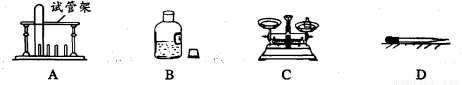
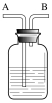
(3)用锌和稀硫酸制取氢气。己知氢气密度比空气小且难溶于水,提供装置如图。
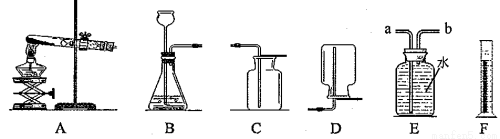
①应选择的制取和收集装置为______(填编号)。
②若用排水法收集并测定气体的体积,则应选用的装置为________。
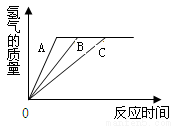
(4)探究影响锌与稀硫酸反应快慢的因素。反应过程中,用前10min内收集的氢气体积来比较反应的快慢。控制其他条件相同,进行下表三组实验,获得数据如下表。
实验编号 | 试剂 | 前 10 min 内产生的氢气体积(mL) | |
不同纯度的锌 | 不同浓度的稀硫酸 | ||
a | 纯锌 | 30 mL 30 % | 564.3 |
b | 含杂质的锌 | 30 mL 30 % | 634.7 |
c | 纯锌 | 30 mL 20 % | 449.3 |
①比较实验 a 和实验 b ,可以得到的结论是________________________。
②为了研究硫酸浓度对反应快慢的影响,需比较实验__________(填编号)。
(本题共9分)水泥厂新进一批石灰石原料,该厂化验室为了测定石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水)有关实验数据如下表:
反应前 | 反应后 | ||
实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
200.0g | 18.0 g | 211.4 g | |
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为 。
(2)求该石灰石中碳酸钙的质量分数(结果保留一位小数,写出计算过程。) 。