题目内容
5.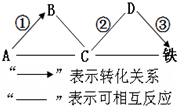 A、B、C、D分别为氧化铁、盐酸、氢氧化钙、碳酸钙中的一种,它们之间的反应或转化关系如图(部分物质和反应条件已略去).其中说法不正确的是( )
A、B、C、D分别为氧化铁、盐酸、氢氧化钙、碳酸钙中的一种,它们之间的反应或转化关系如图(部分物质和反应条件已略去).其中说法不正确的是( )| A. | C物质是盐酸 | |
| B. | 反应①的化学方程式可以是:CO2+Ca(OH)2═CaCO3↓+H2O | |
| C. | 反应②中所得溶液呈浅绿色 | |
| D. | 反应③中D物质可发生还原反应得到铁 |
分析 根据A、B、C、D分别为氧化铁、盐酸、氢氧化钙、碳酸钙中的一种,D会转化成铁,所以D是氧化铁,C会与铁和氧化铁反应,所以C是盐酸,A会转化成B,所以A是氢氧化钙,B是碳酸钙,然后将推出的物质进行验证结合选项判断即可.
解答 解:A、B、C、D分别为氧化铁、盐酸、氢氧化钙、碳酸钙中的一种,D会转化成铁,所以D是氧化铁,C会与铁和氧化铁反应,所以C是盐酸,A会转化成B,所以A是氢氧化钙,B是碳酸钙,经过验证,推导正确,所以A是氢氧化钙,B是碳酸钙,C是盐酸,D是氧化铁,因此:
A、通过推导可知,C物质是盐酸,说法正确;
B、反应①是氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O,说法正确;
C、反应②是氧化铁和盐酸反应生成氯化铁和水,所得溶液为黄色,故说法错误;
D、反应③中氧化铁失去氧发生还原反应,故说法正确;
故选项为:C.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.分类是学习化学的一种重要科学方法.下列物质分类正确的是( )
| A. | 常见的混合物:空气、冰水混合物 | B. | 常见的碱:纯碱、熟石灰 | ||
| C. | 常见的氧化物:水、生石灰 | D. | 常见的易燃物:汽油、浓硫酸 |
20.生活中的下列变化,一定发生了化学变化的是( )
| A. |  风力发电 风力发电 | B. |  海水晒盐 海水晒盐 | C. |  酿制米酒 酿制米酒 | D. |  石油炼制 石油炼制 |
10.氢氧化钠是一种重要的化工原料,也是实验室中常见的一种试剂,氢氧化钠必须密封保存,因为易与空气中二氧化碳发生化学反应而变质,用化学方程式表示变质原因2NaOH+CO2═Na2CO3+H2O.
下面是几位同学对一瓶氢氧化钠固体成分进行的探究:
探究一:确定一瓶氢氧化钠固体是否变质
小强方案:
探究二:确定氢氧化钠固体变质的程度
小刚方案:
小刚实验方案中滴入过量的CaCl2溶液目的是全部除去溶液中的Na2CO3
探究三:定量分析部分变质的氢氧化钠固体中氢氧化钠的含量
1、下面是小明和小军两位同学不同的设计实验方案:
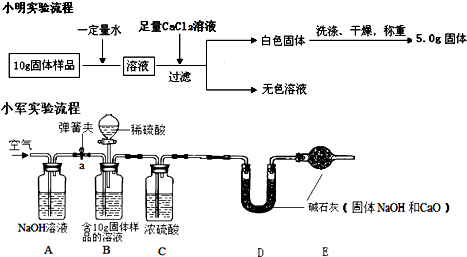
通过小明实验方案计算出样品中氢氧化钠的含量(写出计算过程)
2、小军实验步骤如下
①检查好装置气密性,装好药品后连接并固定好装置
②打开弹簧夹a,通入一段时间的空气,再称量D装置质量记录为100g
③关闭弹簧夹a,打开B装置中的分液漏斗,滴入稀硫酸,直到瓶内无气泡产生.
④打开弹簧夹a,继续通入一段时间空气,再称量D装置质量记录为102.2g
…
实验分析:
(1)在小军实验中A装置作用是除去空气中的CO2,防止其被D吸收,
(2)实验步骤④中,继续通入一段时间空气的目的是将反应生成的CO2全部排出被D吸收,
(3)如果缺装置C,最终所测得氢氧化钠的含量将会偏低(填“偏高”、“不变”、或者“偏低”)
下面是几位同学对一瓶氢氧化钠固体成分进行的探究:
探究一:确定一瓶氢氧化钠固体是否变质
小强方案:
| 实验操作 | 实验现象 | 结论 |
| 取少量样品于试管中,加入一定量水,样品全溶解后,滴加足量的稀盐酸(稀硫酸)(填一种溶液名称) | 有气泡产生 | 氢氧化钠已变质 |
小刚方案:
| 实验操作 | 实验现象 | 结论 |
| ①取少量样品于试管中,加入一定量水后,样品全溶解后,滴加过量的CaCl2溶液 | 产生白色沉淀 | 氢氧化钠固体部分 变质 |
| ②静置后取上层清液于试管中,滴入2滴酚酞试液 | 溶液变红 |
探究三:定量分析部分变质的氢氧化钠固体中氢氧化钠的含量
1、下面是小明和小军两位同学不同的设计实验方案:

通过小明实验方案计算出样品中氢氧化钠的含量(写出计算过程)
2、小军实验步骤如下
①检查好装置气密性,装好药品后连接并固定好装置
②打开弹簧夹a,通入一段时间的空气,再称量D装置质量记录为100g
③关闭弹簧夹a,打开B装置中的分液漏斗,滴入稀硫酸,直到瓶内无气泡产生.
④打开弹簧夹a,继续通入一段时间空气,再称量D装置质量记录为102.2g
…
实验分析:
(1)在小军实验中A装置作用是除去空气中的CO2,防止其被D吸收,
(2)实验步骤④中,继续通入一段时间空气的目的是将反应生成的CO2全部排出被D吸收,
(3)如果缺装置C,最终所测得氢氧化钠的含量将会偏低(填“偏高”、“不变”、或者“偏低”)
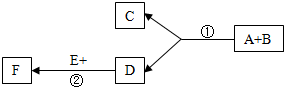 现有A~F六种九年级化学常见物质,其中A、C都是白色固体,D是常见的气体,E是固体火柴头的成分之一,E在D中燃烧会产生大量白烟F,B是黑色固体,它们的转化关系如图.
现有A~F六种九年级化学常见物质,其中A、C都是白色固体,D是常见的气体,E是固体火柴头的成分之一,E在D中燃烧会产生大量白烟F,B是黑色固体,它们的转化关系如图.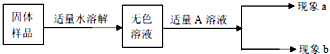
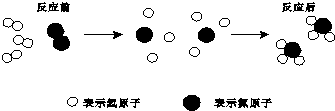
 属于单质(填“单质”或“化合物”).
属于单质(填“单质”或“化合物”). 二氧化锰和硫酸铜溶液都可作为过氧化氢分解的催化剂.在一节化学实验课上,小花同学向10g过氧化氢中加入1.65g溶质质量分数为10%的硫酸铜溶液.实验过程中溶液总质量与反应时间的关系如图所示.求:
二氧化锰和硫酸铜溶液都可作为过氧化氢分解的催化剂.在一节化学实验课上,小花同学向10g过氧化氢中加入1.65g溶质质量分数为10%的硫酸铜溶液.实验过程中溶液总质量与反应时间的关系如图所示.求: