题目内容
18.我县某中学化学实验小组在整理试验台时,看到一些试剂的放置如下,你认为正确的是( )| A. | 盛放氢氧化钠溶液的试剂瓶敞口放置 | |
| B. | 盛浓硫酸的试剂瓶敞口放置 | |
| C. | 生石灰放在敞口的小烧杯中 | |
| D. | 浓盐酸放置在密封的试剂瓶中 |
分析 A、氢氧化钠溶液能与二氧化碳反应.
B、浓硫酸具有较强的吸水性.
C、生石灰能与水反应.
D、浓盐酸具有较强的挥发性.
解答 解:A、固体氢氧化钠易潮解,且能与空气中的二氧化碳反应反应.故用橡皮塞密封保存,故此选项错误.
B、浓硫酸具有较强的吸水性,所以应储存在密闭的细口瓶中,故此选项错误.
C、生石灰能与水反应,因此应密封保存,故此选项错误.
D、浓盐酸具有较强的挥发性,所以应密封保存在细口瓶中,故此选项正确.
故选D.
点评 此题是药品储存的有关考查题,解题的关键是了解所储存物质的特性,属基础性知识考查题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.观察下面反应的微观示意图,下列说法错误的是( )


| A. | 化学反应前后各元素的化合价均保持不变 | |
| B. | W物质中碳元素的质量分数为80% | |
| C. | 参加反应的X、Y两物质的粒子个数比为3:4 | |
| D. | 该反应属于置换反应 |
6. 如图不能正确表示对应变化关系的是( )
如图不能正确表示对应变化关系的是( )
 如图不能正确表示对应变化关系的是( )
如图不能正确表示对应变化关系的是( )| A. | 化学反应中,原子总数Y随反应时间X的变化关系 | |
| B. | 恒温,向硝酸钾饱和溶液中加入KNO3,溶质的质量分数Y随硝酸钾加入量X的变化 | |
| C. | 向碳酸钠溶液中加稀盐酸,溶液的质量Y随稀盐酸加入量X的变化 | |
| D. | 二氧化锰与氯酸钾共热,二氧化锰在反应时的质量Y随时间X的变化 |
6.“低钠盐”可以控制钠的摄入量从而防治高血压等疾病.制备“低钠盐”是在食盐中用NaCl按照配方比例添加食用KCl.国内某些生产厂家为改变“低钠盐”口味还会加入少量镁盐(仅限MgSO4或MgCl2).
(1)测得某“低钠盐”样品a中只含有NaCl和KCl,该样品中的NaCl和KCl溶于水时解离出的阴离子都是Cl-(填离子符号).
(2)探究某“低钠盐”样品b中是否添加有镁盐,以及添加的是何种镁盐?
【猜想】I、不含镁盐Ⅱ、含有硫酸镁Ⅲ、含有氯化镁
【进行实验】

(3)请完成如表(已知BaSO4是难溶于水和酸的白色固体):
(1)测得某“低钠盐”样品a中只含有NaCl和KCl,该样品中的NaCl和KCl溶于水时解离出的阴离子都是Cl-(填离子符号).
(2)探究某“低钠盐”样品b中是否添加有镁盐,以及添加的是何种镁盐?
【猜想】I、不含镁盐Ⅱ、含有硫酸镁Ⅲ、含有氯化镁
【进行实验】

(3)请完成如表(已知BaSO4是难溶于水和酸的白色固体):
| 假设和现象 | 判断和化学方程式 | |
| ① | 若现象a为白色沉淀 | 则猜想I不成立. |
| ② | 若现象a为产生白色沉淀, 现象b为无明显现象. | 则猜想Ⅲ成立.写出无色溶液B与硝酸中和反 应的化学方程式NaOH+HNO3=NaNO3+H2O. |
| ③ | 若现象a、b均 为:产生白色沉淀 | 则猜想Ⅱ成立.写出无色溶液B与硝酸钡溶液 反应的化学方程式Ba(NO3)2+Na2SO4=BaSO4↓+2NaNO3. |



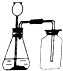 写出实验室用如图装置制取气体的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑或CaCO3+2HCl=CaCl2+H2O+CO2↑,在不增减仪器的情况下,略加改动还可以制取的气体是氢气.
写出实验室用如图装置制取气体的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑或CaCO3+2HCl=CaCl2+H2O+CO2↑,在不增减仪器的情况下,略加改动还可以制取的气体是氢气.