题目内容
有某固体混合物,已知该混合物中可能含有FeCl3、Na2SO4、NH4NO3、CuSO4四种物质中的两种或多种.按图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全反应).
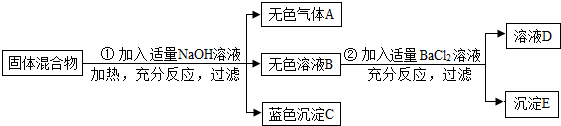
试根据实验过程和发生的现象填写以下空白:
(1)用湿润的红色石蕊试纸测试气体A,试纸变 色.
(2)固体混合物里.上述四种物质中,肯定不存在的物质是 .
(3)实验证明,在溶液D中,肯定存在的酸根离子是(写离子符号) .
(4)实验过程②中发生反应的化学方程式为 .
(5)固体混合物里,上述四种物质中,还不能确定存在的物质是(写化学式) ,得此结论的理由是 .

试根据实验过程和发生的现象填写以下空白:
(1)用湿润的红色石蕊试纸测试气体A,试纸变
(2)固体混合物里.上述四种物质中,肯定不存在的物质是
(3)实验证明,在溶液D中,肯定存在的酸根离子是(写离子符号)
(4)实验过程②中发生反应的化学方程式为
(5)固体混合物里,上述四种物质中,还不能确定存在的物质是(写化学式)
考点:物质的鉴别、推断,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:混合物组成的推断题
分析:(1)由混合物的可能组成中能与氢氧化钠反应生成无色气体的物质只有硝酸铵,二者反应生成氨气;该气体遇水呈碱性,可使湿润的红色石蕊试纸变蓝;
(2)氯化铁与氢氧化钠可反应生成红褐色沉淀氢氧化铁;
(3)硫酸铜与氢氧化钠反应可生成氢氧化铜蓝色沉淀;所以混合物中除了含有硝酸铵,还一定含有硫酸铜;硝酸铵与氢氧化钠反应生成硝酸钠、水、氨气,硫酸铜与氢氧化钠反应生成氢氧化铜和硫酸钠,所以溶液B中含有硝酸钠和硫酸钠;然后根据二者与氯化钡的反应判断溶液D的组成,进而判断存在的酸根离子;
(4)根据复分解反应的规律,结合(3)的分析,可知硫酸钠与氯化钡可反应,而硝酸钠不反应,写出反应的化学方程式;
(5)根据实验现象逐一分析混合物中不能确定的物质是硫酸钠,因为CuSO4一定存在,与NaOH反应后生成的Na2SO4在溶液B中已经能与BaCl2反应生成沉淀.
(2)氯化铁与氢氧化钠可反应生成红褐色沉淀氢氧化铁;
(3)硫酸铜与氢氧化钠反应可生成氢氧化铜蓝色沉淀;所以混合物中除了含有硝酸铵,还一定含有硫酸铜;硝酸铵与氢氧化钠反应生成硝酸钠、水、氨气,硫酸铜与氢氧化钠反应生成氢氧化铜和硫酸钠,所以溶液B中含有硝酸钠和硫酸钠;然后根据二者与氯化钡的反应判断溶液D的组成,进而判断存在的酸根离子;
(4)根据复分解反应的规律,结合(3)的分析,可知硫酸钠与氯化钡可反应,而硝酸钠不反应,写出反应的化学方程式;
(5)根据实验现象逐一分析混合物中不能确定的物质是硫酸钠,因为CuSO4一定存在,与NaOH反应后生成的Na2SO4在溶液B中已经能与BaCl2反应生成沉淀.
解答:解:(1)由混合物的可能组成中能与氢氧化钠反应生成无色气体的物质只有硝酸铵,二者反应生成氨气;该气体遇水呈碱性,可使湿润的红色石蕊试纸变蓝;
故答案为:蓝;
(2)氯化铁与氢氧化钠可反应生成红褐色沉淀氢氧化铁;根据题意:过程中所有发生的反应都恰好完全反应,而步骤①中得到蓝色沉淀,并无红褐色沉淀产生,说明一定没有氯化铁;
故答案为:FeCl3;
(3)硫酸铜与氢氧化钠反应可生成氢氧化铜蓝色沉淀;所以混合物中除了含有硝酸铵,还一定含有硫酸铜;
硝酸铵与氢氧化钠反应生成硝酸钠、水、氨气,硫酸铜与氢氧化钠反应生成氢氧化铜和硫酸钠,所以溶液B中含有硝酸钠和硫酸钠;
其中硫酸钠与氯化钡可反应生成氯化钠和硫酸钡沉淀,硝酸钠与氯化钡不反应,所以溶液D中,肯定存在的酸根离子是硝酸根离子、氯离子;
故答案为:NO3-、Cl-;
(4)由上述(3)的分析,可推断出溶液B中含有硝酸钠和硫酸钠;硝酸钠与氯化钡混合无气体、水、沉淀产生,故二者不反应,硫酸钠与氯化钡可反应生成氯化钠和硫酸钡沉淀,方程式是Na2SO4+BaCl2═BaSO4↓+2NaCl;
故答案为:Na2SO4+BaCl2═BaSO4↓+2NaCl;
(5)根据步骤①有无色气体产生、蓝色沉淀生成,可知混合物中一定含有硝酸铵、硫酸铜,一定不含氯化铁;因为CuSO4一定存在,与NaOH反应后生成的Na2SO4在溶液B中已经能与BaCl2反应生成沉淀,故无法确定固体混合物里是否含有硫酸钠;
故答案为:Na2SO4;理由:因为NaOH和CuSO4反应也能生成Na2SO4.
故本题答案为:
(1)蓝;
(2)氯化铁;
(3)NO3-、Cl-;
(4)Na2SO4+BaCl2═BaSO4↓+2NaCl;
(5)因为NaOH和CuSO4反应也能生成Na2SO4.
故答案为:蓝;
(2)氯化铁与氢氧化钠可反应生成红褐色沉淀氢氧化铁;根据题意:过程中所有发生的反应都恰好完全反应,而步骤①中得到蓝色沉淀,并无红褐色沉淀产生,说明一定没有氯化铁;
故答案为:FeCl3;
(3)硫酸铜与氢氧化钠反应可生成氢氧化铜蓝色沉淀;所以混合物中除了含有硝酸铵,还一定含有硫酸铜;
硝酸铵与氢氧化钠反应生成硝酸钠、水、氨气,硫酸铜与氢氧化钠反应生成氢氧化铜和硫酸钠,所以溶液B中含有硝酸钠和硫酸钠;
其中硫酸钠与氯化钡可反应生成氯化钠和硫酸钡沉淀,硝酸钠与氯化钡不反应,所以溶液D中,肯定存在的酸根离子是硝酸根离子、氯离子;
故答案为:NO3-、Cl-;
(4)由上述(3)的分析,可推断出溶液B中含有硝酸钠和硫酸钠;硝酸钠与氯化钡混合无气体、水、沉淀产生,故二者不反应,硫酸钠与氯化钡可反应生成氯化钠和硫酸钡沉淀,方程式是Na2SO4+BaCl2═BaSO4↓+2NaCl;
故答案为:Na2SO4+BaCl2═BaSO4↓+2NaCl;
(5)根据步骤①有无色气体产生、蓝色沉淀生成,可知混合物中一定含有硝酸铵、硫酸铜,一定不含氯化铁;因为CuSO4一定存在,与NaOH反应后生成的Na2SO4在溶液B中已经能与BaCl2反应生成沉淀,故无法确定固体混合物里是否含有硫酸钠;
故答案为:Na2SO4;理由:因为NaOH和CuSO4反应也能生成Na2SO4.
故本题答案为:
(1)蓝;
(2)氯化铁;
(3)NO3-、Cl-;
(4)Na2SO4+BaCl2═BaSO4↓+2NaCl;
(5)因为NaOH和CuSO4反应也能生成Na2SO4.
点评:解题时利用物质间的反应规律、抓住反应中所出现的现象,寻找突破口(即物质的特性或反应时的特殊现象等),细心地全面思考、推断即可,该类题能很好的考查学生分析、解决问题的能力.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
下列实验操作符合规范的是( )
A、 |
B、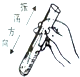 |
C、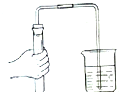 |
D、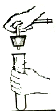 |
道尔顿的原子学说曾起了很大作用,他的学说中,包含有下述三个论点,用现在的观点看,你认为这三个论点中,不确切的是( )
①原子是不能再分的粒子.
②同种元素的原子的各种性质和质量都相同.
③原子是微小的实心球体.
①原子是不能再分的粒子.
②同种元素的原子的各种性质和质量都相同.
③原子是微小的实心球体.
| A、③ | B、①③ | C、②③ | D、①②③ |
下列说法正确的是( )
| A、蔬菜切碎后再洗不会造成维生素流失 |
| B、糖类都有甜味,是人从食物中摄取的重要营养成分之一 |
| C、油脂的组成元素与淀粉相同,分子组成和结构也相同 |
| D、可溶性的重金属盐能使蛋白质失去原有的生理功能,误食会使人中毒 |
以下属于废物回收标志的是( )
A、 |
B、 |
C、 |
D、 |
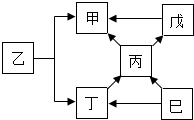 甲~己六种物质的转化关系如图所示.已知甲能使澄清石灰水变浑浊;己是无色溶液,能在某种黑色固体物质催化下,生成可供给呼吸的气体.(部分反应物、产物及反应条件已略去,“→”表示物质之间能发生转化)
甲~己六种物质的转化关系如图所示.已知甲能使澄清石灰水变浑浊;己是无色溶液,能在某种黑色固体物质催化下,生成可供给呼吸的气体.(部分反应物、产物及反应条件已略去,“→”表示物质之间能发生转化)