题目内容
11.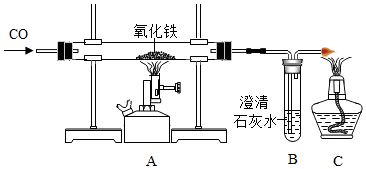 炼铁的原理是利用一氧化碳与氧化铁反应.在实验室里,可以利用如图所示的装置进行实验,请回答下列问题.
炼铁的原理是利用一氧化碳与氧化铁反应.在实验室里,可以利用如图所示的装置进行实验,请回答下列问题.(1)实验开始时,应B;
A.先加热再通人CO B.先通入CO再加热
(2)实验进行时,A处出现的现象为红棕色粉末变成了黑色,发生反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,B处发生反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O;
(3)C处点燃酒精灯的目的是除去多余的CO,防止污染空气(或防止中毒).
分析 (1)根据实验中的注意事项来分析;
(2)根据化学反应的原理来书写化学方程式,根据物质的颜色变化解答;
(3)尾气中含有一氧化碳.
解答 解:(1)因为一氧化碳具有可燃性,点燃或加热一氧化碳与空气的混合物可能引起爆炸,故加热前要先通入一氧化碳,排除空气防止爆炸;故填:B;
(2)在高温的条件下,一氧化碳与氧化铁反应生成铁和二氧化碳,会观察到红棕色粉末变成了黑色;二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水;故填:红棕色粉末变成了黑色;Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;Ca(OH)2+CO2=CaCO3↓+H2O;
(3)由于一氧化碳有毒,如果直接排放到空气中,会造成污染,可用点燃的方法将一氧化碳燃烧掉,防止污染空气;故填:除去多余的CO,防止污染空气(或防止中毒).
点评 了解一氧化碳还原氧化铁的反应原理、操作步骤、注意事项、尾气处理等知识,才能结合题意灵活分析解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.小勇同学根据已有的化学知识,向家人提出了下列建议,其中不合理的是( )
| A. | 用燃烧闻气味的方法鉴别棉纤维和羊毛制品 | |
| B. | 用加热煮沸的方法降低水的硬度 | |
| C. | 用煤炉取暖时,为防止热量散失,应紧闭门窗 | |
| D. | 胃酸过多时,可服用适量的小苏打 |
2.在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示:
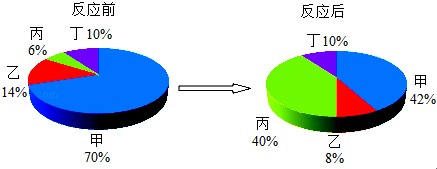
下列说法正确的是( )

下列说法正确的是( )
| A. | 丙可能是单质 | |
| B. | 该反应是化合反应 | |
| C. | 在该反应中丁一定没有参加化学反应 | |
| D. | 甲和乙的质量之和一定等于生成丙的质量 |
19.金属材料在人类活动中具有广泛的应用.下列有关金属的说法中,不正确的是( )
| A. | 铜质插头是利用铜的导电性 | B. | 钨制灯丝是利用钨的熔点低 | ||
| C. | 铝制成铝箔是利用铝的延展性 | D. | 铁锅炒菜是利用铁的导热性 |
16.失去标签的三瓶无色液体,分别是稀硫酸、蒸馏水、氢氧化钠溶液,一次性就能把它们区别开的试剂是( )
| A. | 无色酚酞试液 | B. | 硝酸钙溶液 | C. | 氯化钡溶液 | D. | 紫色石蕊试液 |