题目内容
3. 市场上某补钙剂的说明书如右图所示:
市场上某补钙剂的说明书如右图所示:(已知葡萄糖酸钙的相对分子质量是430)
(1)葡萄糖酸钙[(C6H11O7)2Ca]中钙元素的质量分数为9.3%;
(2)此补钙剂中每片钙片含葡萄糖酸钙的质量分数为8%;
(3)每天能补充钙的质量为0.037g.
分析 (1)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
(2)根据题意,每片含葡萄糖酸钙0.2g,每片的质量为2.5g,进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)葡萄糖酸钙[(C6H11O7)2Ca]中钙元素的质量分数为$\frac{40}{430}×$100%≈9.3%.
(2)每片含葡萄糖酸钙0.2g,每片的质量为2.5g,则每片含葡萄糖酸钙的质量为$\frac{0.2g}{2.5g}$×100%=8%.
(3)每日2次,每次1片,每天能补充钙的质量为0.2g×($\frac{40}{430}×$100%)×2≈0.037g.
故答案为:(1)9.3%;(2)8%;(3)0.037g.
点评 本题难度不大,考查同学们结合标签新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
2.2014年12月7日11时26分,我国在太原卫星发射中心用长征四号乙运载火箭,成功经中巴地球资源卫星04星04星发射升空.我国运载火箭的动力是由高氯酸按(NH4ClO4)分解所提供的,反应的化学方程式为2NH4ClO4$\frac{\underline{\;\;△\;\;}}{\;}$N2↑+Cl2↑+4X↑+2O2↑.下列有关说法正确的是( )
| A. | X的化学式为HCl | |
| B. | 上述反应属于分解反应 | |
| C. | N2和O2都是空气的成分,其中O2是空气中含量最多的气体 | |
| D. | NH4ClO4中氮元素的质量分数为30% |
3.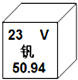 2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13).钒元素的相关信息如图.下列有关钒的说法错误的是( )
2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13).钒元素的相关信息如图.下列有关钒的说法错误的是( )
 2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13).钒元素的相关信息如图.下列有关钒的说法错误的是( )
2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13).钒元素的相关信息如图.下列有关钒的说法错误的是( )| A. | 相对原子质量为50.94g | B. | 原子的核电荷数是23 | ||
| C. | 元素符号是V | D. | 属于金属元素 |
7.水是一切生物生存所必需的,我们应该了解有于水的一些知识.
(1)硬水给生活和生产带来很多麻烦,生活中可用肥皂水来区分硬水和软水;
(2)我国是淡水资源非常有限的国家,爱护水资源是每个公民的责任和义务.下列行为属于浪费水的是AD(填字母编号);
A.洗手擦香皂时不关上水龙头 B.用洗菜水浇花
C.用洗衣水冲厕所 D.用自来水不断为西瓜冲水降温.
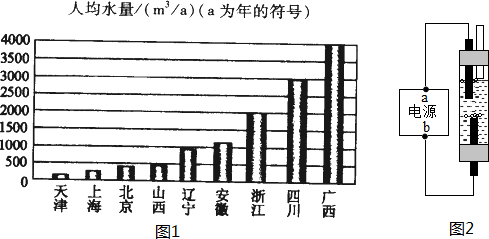
(3)资料一:我国部分省市人均水量图(如图1)
资料二:水资源紧缺指标
上述资料显示,北京属于典型的极度缺水城市,我们每个人都应该节约用水,你家中的节水办法是用洗菜水浇花(写出一条即可).
(4)如图2是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气(Cl2),该反应的文字表达式为氯化钠+水$\stackrel{通电}{→}$氢氧化钠+氢气+氯气;从能量变化角度看,该反应将电能转化为化学能.

(1)硬水给生活和生产带来很多麻烦,生活中可用肥皂水来区分硬水和软水;
(2)我国是淡水资源非常有限的国家,爱护水资源是每个公民的责任和义务.下列行为属于浪费水的是AD(填字母编号);
A.洗手擦香皂时不关上水龙头 B.用洗菜水浇花
C.用洗衣水冲厕所 D.用自来水不断为西瓜冲水降温.
(3)资料一:我国部分省市人均水量图(如图1)
资料二:水资源紧缺指标
| 紧 缺 性 | 轻度缺水 | 中度缺水 | 重度缺水 | 极度缺水 |
| 人均水量(m3/a) | 1700-3000 | 1000-1700 | 500-1000 | <500 |
(4)如图2是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气(Cl2),该反应的文字表达式为氯化钠+水$\stackrel{通电}{→}$氢氧化钠+氢气+氯气;从能量变化角度看,该反应将电能转化为化学能.
15.对有关实验现象的描述不正确的是( )
| A. | 硫在氧气中燃烧发出明亮蓝紫色火焰 | |
| B. | 浓盐酸敞口放置在空气中瓶口猫“白雾” | |
| C. | 铁丝在氧气中燃烧生成白色固体四氧化三铁 | |
| D. | 红磷在氧气中燃烧产生白烟 |
12.符合以下四位同学所描述的化学式可能是( )


| A. | H2O | B. | O2 | C. | MgO | D. | HClO |
 眼镜是人们常用的护眼工具,如图是一款变色眼镜的示意图:
眼镜是人们常用的护眼工具,如图是一款变色眼镜的示意图: