题目内容
16.从2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O中获取的信息错误的是( )| A. | 在反应前后,元素的种类没有变化 | |
| B. | 在常温下氢气与氧气混合就可以发生反应 | |
| C. | 4g氢气与32g氧气完全反应,可以生成36g水 | |
| D. | 在反应前后,氢原子和氧原子的数目都没有改变 |
分析 根据质量守恒定律和化学方程式的实际应用,A和C是质量守恒的宏观说法,D是微观说法.氢气和氧气的反应是在点燃条件下才可以发生,故B错误.
解答 解:A、反应前氢气和氧气中含有有氢元素和氧元素,反应后水中含有氢元素和氧元素,故A正确;
B、从以上方程式中可知氢气与氧气在点燃的条件下才能反应,故B错误;
C、从以上方程式中可知,每4份质量的氢气和32份质量的氧气完全反应可以生成36份质量的水,故C正确;
D、从以上方程式中可知,反应前氢原子有4个,氧气有2个,反应后氢原子有4个,氧原子又2个,故D正确;
故选B
点评 化学方程式是最重要的化学用语之一,掌握化学方程式的含义、了解方化学程式的读法是正确解答此类题的关键.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
18.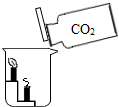 通过实验探究可获得较多的化学知识,对如图所示的实验分析错误的是( )
通过实验探究可获得较多的化学知识,对如图所示的实验分析错误的是( )
 通过实验探究可获得较多的化学知识,对如图所示的实验分析错误的是( )
通过实验探究可获得较多的化学知识,对如图所示的实验分析错误的是( )| A. | 两支蜡烛自下而上依次熄灭 | B. | 二氧化碳不能燃烧 | ||
| C. | 二氧化碳的密度比空气大 | D. | 二氧化碳支持燃烧 |
7.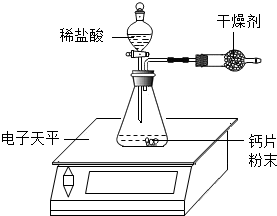 小明为了测定某钙片中碳酸钙的质量分数,用如图装置进行如下实验:
小明为了测定某钙片中碳酸钙的质量分数,用如图装置进行如下实验:
①取研碎后的钙片4克,导入气密性良好的锥形瓶中,然后在分液漏斗中加入适量的稀盐酸,置于电子天平上测出装置总质量.
②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量.
③整理相关数据如表所示,计算出钙片中碳酸钙的质量分数.
1)该实验中,对装置中的固态干燥剂的性质有何要求?能吸收水但不吸收二氧化碳
(2)反应前容器内是空气(密度为ρ1),反应后全部是二氧化碳(密度为ρ2),则反应前后容器(容积为V)内的气体质量差为m为(ρ2-ρ1)V.(用字母表示,反应物的体积忽略不计)
(3)小明查阅有关数据后,计算出反应前后容器内的气体质量差m为0.22克,结合表中数据,计算该钙片中碳酸钙的质量分数.(CaCO3+2HCl=CaCl2+H2O+CO2↑).钙片中的其它成分不与盐酸反应.
 小明为了测定某钙片中碳酸钙的质量分数,用如图装置进行如下实验:
小明为了测定某钙片中碳酸钙的质量分数,用如图装置进行如下实验:①取研碎后的钙片4克,导入气密性良好的锥形瓶中,然后在分液漏斗中加入适量的稀盐酸,置于电子天平上测出装置总质量.
②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量.
③整理相关数据如表所示,计算出钙片中碳酸钙的质量分数.
| 反应前总质量(克) | 275.58 |
| 反应后总质量(克) | 274.92 |
| 反应前后总质量差(克) | 0.66 |
| 容器内气体质量差(克) | m |
(2)反应前容器内是空气(密度为ρ1),反应后全部是二氧化碳(密度为ρ2),则反应前后容器(容积为V)内的气体质量差为m为(ρ2-ρ1)V.(用字母表示,反应物的体积忽略不计)
(3)小明查阅有关数据后,计算出反应前后容器内的气体质量差m为0.22克,结合表中数据,计算该钙片中碳酸钙的质量分数.(CaCO3+2HCl=CaCl2+H2O+CO2↑).钙片中的其它成分不与盐酸反应.
4.下列化学反应属于复分解反应是( )
| A. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O | B. | 3Fe+2CO2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | ||
| C. | NaOH+HCl═NaCl+H2O | D. | H2CO3═CO2↑+H2O |
11.保护环境,节约资源,从我做起.下列做法符合这一理念的是( )
| A. | 生活污水直接排放到河涌中 | B. | 垃圾分类回收处理 | ||
| C. | 自来水价格便宜,可以尽情使用 | D. | 废旧电池掩埋在土壤中 |
1.碲(Te)被誉为“现代工业、国防与尖端技术的维生素,创造人间奇迹的桥梁”.实验室模拟提取碲的一个实验是:取某含碲溶液于烧瓶中,加入适量NaC1,加热到一定温度,持续通入SO2,待反应一定时间,过滤得到粗碲.
(1)反应的总化学方程式为:TeOSO4+2SO2+3X$\frac{\underline{\;\;△\;\;}}{\;}$Te↓+3H2SO4,则X为H2O(填化学式).
(2)为探究获得较高粗碲沉淀率的反应条件,某研究小组在控制NaC1浓度和SO2流量不变的条件下,进行下述对比试验,数据如下:
①该小组研究的反应条件是温度和反应时间.
②实验a和b的目的是比较相同时间,不同的反应温度对粗碲沉淀率的影响.
③在上述四组实验中,最佳的反应条件是80℃和2.0h.
④为了提升设备利用效率和节约能源,可进一步优化反应条件测定粗碲沉淀率.若再设计对比实验,选择的反应条件还可以是A(填选项).
A.80℃,1.5h B.80℃,2.5h C.70℃,2.0h D.95℃,2.0h.
(1)反应的总化学方程式为:TeOSO4+2SO2+3X$\frac{\underline{\;\;△\;\;}}{\;}$Te↓+3H2SO4,则X为H2O(填化学式).
(2)为探究获得较高粗碲沉淀率的反应条件,某研究小组在控制NaC1浓度和SO2流量不变的条件下,进行下述对比试验,数据如下:
| 实验 | 温度/℃ | 反应时间/h | 粗蹄沉淀率 |
| a | 65 | 3.0 | 65.0 |
| b | 80 | 3.0 | 98.9 |
| c | 80 | 2.0 | 98.9 |
| d | 90 | 2.0 | 97.0 |
②实验a和b的目的是比较相同时间,不同的反应温度对粗碲沉淀率的影响.
③在上述四组实验中,最佳的反应条件是80℃和2.0h.
④为了提升设备利用效率和节约能源,可进一步优化反应条件测定粗碲沉淀率.若再设计对比实验,选择的反应条件还可以是A(填选项).
A.80℃,1.5h B.80℃,2.5h C.70℃,2.0h D.95℃,2.0h.
8.下列几种常见的饮料中,不含有机物的可能是( )
| A. | 矿泉水 | B. | 果汁 | C. | 啤酒 | D. | 牛奶 |
5.生活中某些物质的pH近似为:西瓜汁5.8、苹果汁3.1、泡菜3.4、鸡蛋清7.6,其中酸性最强的是( )
| A. | 苹果汁 | B. | 泡菜 | C. | 西瓜汁 | D. | 鸡蛋清 |
6.自然界中的物质大多数是化合物.下列物质属于氧化物的是( )
| A. | KCl | B. | CuSO4 | C. | MnO2 | D. | HNO3 |