题目内容
2.根据下列实验图示分析问题:
(1)分别写出上述三个反应的化学方程式:
硫的燃烧硫+氧气$\stackrel{点燃}{→}$二氧化硫;
镁带的燃烧镁+氧气$\stackrel{点燃}{→}$氧化镁;
铁丝的燃烧铁+氧气$\stackrel{点燃}{→}$四氧化三铁;
(2)上述三个反应都是物质与氧气发生的反应,它们都属于氧化反应.氧气在氧化反应中提供氧,它具有氧化性.若从元素的化合价变化分析,氧元素在上述反应中反应后,氧元素的化合价降低了.
(3)通过类比、分析反应2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl发现Cl2(填化学式)物质也具有氧化性.
分析 (1)根据硫、镁带、铁与氧气点燃反应原理书写方程式;
(2)物质与氧气发生的反应是氧化反应,并分析氧元素化合价变化;
(3)由(2)可知:元素化合价升高则具有氧化性,并结合化学反应中元素化合价的变化回答.
解答 解:
(1)硫在氧气中燃烧生成二氧化硫,反应的文字表达式是:硫+氧气$\stackrel{点燃}{→}$二氧化硫;镁带和氧气在点燃的条件下生成氧化镁,反应的文字表达式是:镁+氧气$\stackrel{点燃}{→}$氧化镁;铁和氧气在点燃的条件下生成四氧化三铁,反应的文字表达式是:铁+氧气$\stackrel{点燃}{→}$四氧化三铁;
(2)上述三个反应都是物质和氧气的反应,属于氧化反应,氧元素在上述反应中,化合价由反应前的0变成了反应后的-2价,化合价都降低了;
(3)在2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl中,氯元素的化合价由0变成了-1,化合价降低了,而氧化反应中化合价降低的物质有氧化性,所以该反应中具有氧化性的物质是氯气;
故答案为:(1)硫+氧气$\stackrel{点燃}{→}$二氧化硫;镁+氧气$\stackrel{点燃}{→}$氧化镁;铁+氧气$\stackrel{点燃}{→}$四氧化三铁;
(2)氧化反应,反应后,氧元素的化合价降低了;
(3)Cl2
点评 本题主要是一道信息给予题,主要考查对信息的分析、提炼、加工、运用能力,体现了新课标对中考的要求和方向.

练习册系列答案
相关题目
10.下列变化中,属于化学变化的是( )
| A. | 蜡烛燃烧 | B. | 瓷碗破碎 | C. | 碘的升华 | D. | 冰雪消融 |
17.图为某反应的微观模拟示意图.从图中获得的有关信息错误的是( )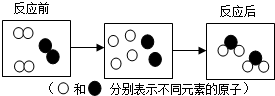

| A. | 原子是化学变化中的最小粒子 | |
| B. | 化学反应前后原子的种类没有改变 | |
| C. | 该化学反应既不是化合反应也不是分解反应 | |
| D. | 分子间存在一定的间隙 |
12.下列实验操作错误的是( )
| A. | 过滤时玻璃棒斜靠在三层滤纸一边 | |
| B. | 过滤时漏斗下端管口紧靠烧杯内壁 | |
| C. | 过滤中玻璃棒的作用是搅拌液体,加快过滤速度 | |
| D. | 在烧杯中溶解粗盐时用玻璃棒搅拌 |

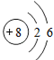 镁原子结构示意图中第一层有两个电子.
镁原子结构示意图中第一层有两个电子.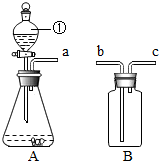 如图装置AB经适当组合可用于氧气、二氧化碳等气体的制备、检验和收集等操作.
如图装置AB经适当组合可用于氧气、二氧化碳等气体的制备、检验和收集等操作.