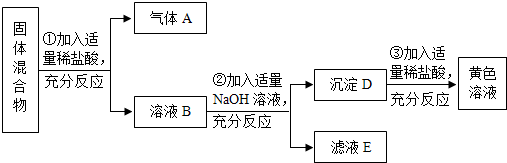
题目内容
2.某同学使用下图所示装置,试验一氧化碳与氧化铁的反应.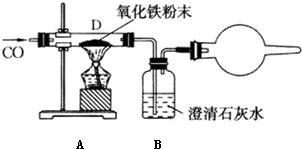
请回答下列有关问题:
(1)有下列实验步骤:①加热;②通人一氧化碳;③停止加热; ④停止通一氧化碳;
实验室用一氧化碳还原氧化铁的步骤为:②①③④,
(2)实验进行一段时间后,A装置中出现的现象为红色粉末变成黑色,化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
(3)B装置中出现的现象为澄清的石灰水变浑浊,说明有二氧化碳生成;化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O
(4)该实验装置有一处缺陷,请你指出并改近没有处理尾气,用气球收集尾气.
分析 (1)根据已有的知识进行分析,一氧化碳还原氧化铁时,要先通入一氧化碳然后加热,实验结束时要先停止加热继续通入一氧化碳至玻璃管冷却,据此解答即可;
(2)A中一氧化碳还原氧化铁生成铁和二氧化碳,根据物质的颜色进行分析;
(3)产生的二氧化碳通入澄清石灰水后会变浑浊;
(4)从一氧化碳过量,排放到空气中会污染空气考虑.
解答 解:(1)一氧化碳还原氧化铁时,要先通入一氧化碳然后加热,否则容易产生爆炸,实验结束时要先停止加热继续通入一氧化碳至玻璃管冷却,否则会导致生成的铁重新被氧化;
(2)在高温的条件下,一氧化碳将氧化铁还原成铁,同时产生二氧化碳,氧化铁是红色的,铁是黑色的;
(3)B装置中澄清的石灰水变浑浊,说明有二氧化碳生成,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水;
(4)如果通入的CO过量,就会沿导管排入大气中,污染空气,所以可用气球收集尾气(或点燃尾气).
故答案为:(1)②①③④;(2)红色粉末变成黑色;3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(3)澄清的石灰水变浑浊;二氧化碳;CO2+Ca(OH)2═CaCO3↓+H2O;(4)没有处理尾气,用气球收集尾气(或点燃尾气等).
点评 本题以一氧化碳还原氧化铁为切入点,考查实验中的注意事项、实验现象、反应原理以及环保的问题,考查知识点全面,但属于基础知识.

练习册系列答案
相关题目
12.闽江某河段水域中氮和磷含量过高,造成水葫芦疯长.这里的“氮”、“磷”是指( )
| A. | 分子 | B. | 原子 | C. | 离子 | D. | 元素 |
7.下列仪器:①量筒 ②试管 ③烧杯 ④燃烧匙,能用酒精灯直接加热的是( )
| A. | ①② | B. | ②④ | C. | ②③④ | D. | ②③ |
7.可以证明烧杯中的溶液是硝酸钾饱和溶液的方法是( )
| A. | 蒸发1g水,有少量固体析出 | |
| B. | 降低温度,有少量固体析出 | |
| C. | 加入少量硝酸钾固体,固体不再溶解 | |
| D. | 升高温度,没有固体析出 |