题目内容
13.某元素的+3价的氧化物中,该元素与氧元素的质量比为13:6,则这种元素相对原子质量为( )| A. | 26 | B. | 52 | C. | 78 | D. | 104 |
分析 化学式中各原子的相对原子质量的总和,就是相对分子质量.根据所给元素的化合价结合氧化物的特点可以写出该物质的化学式,我们可以确定物质组成元素的质量比.由题意可知,某元素的氧化物中该元素与氧元素的质量比为13:6,将氧元素的相对原子质量16代入质量比公式即可得该元素的相对原子质量.
解答 解:设该元素元素符号为R,其化合价为+3,而氧元素的化合价为-2,所以根据化合物正负化合价的代数和为零,可以知道该物质的化学式为:R2O3
设R元素的相对原子质量为x,由化学式R2O3可得
2x:(3×16)=13:6
解得x=52
故选B.
点评 本题重在考查根据物质的化学式,计算物质组成元素的质量比.解本题的关键是正确理解相对分子质量是化学式中各原子的相对原子质量的总和这一概念.

练习册系列答案
相关题目
1.以下是两种物质在一定条件下发生化学反应的微观示意图:(其中○和●分别表示两种不同的原子)
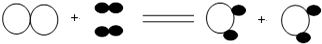
由图可知,下列说法中正确的是( )
(1)该反应属于化合反应 (2)生成物可能是氧化物(3)反应前后原子的个数不变
(4)反应前后分子和原子种类都不变 (5)分子在化学变化中可以再分,而原子不能再分.

由图可知,下列说法中正确的是( )
(1)该反应属于化合反应 (2)生成物可能是氧化物(3)反应前后原子的个数不变
(4)反应前后分子和原子种类都不变 (5)分子在化学变化中可以再分,而原子不能再分.
| A. | (1)(2)(3)(5) | B. | (1)(2)(4)(5) | C. | (1)(3)(4)(5) | D. | (1)(2)(3)(4)(5) |
5.一种原子的核内有6个质和6个中子,另一种原子的核内有6个质子和7个中子,则它们不同的是( )?
| A. | 核电荷数 | B. | 核外电子数 | C. | 原子的质量 | D. | 元素的种类? |
2.下列反应中,不属于分解反应也不属于化合反应的是( )
| A. | 水$\stackrel{通电}{→}$氢气+氧气 | B. | 木炭+氧气$\stackrel{点燃}{→}$二氧化碳 | ||
| C. | 甲烷+氧气$\stackrel{点燃}{→}$二氧化碳+水 | D. | 氯酸钾$\stackrel{加热}{→}$氯化钾+氧气 |