题目内容
4.人类的生活和工农业生产都离不开化学.(1)自来水净化水过程中,使用的净水方法不包括CD(填序号)
A.沉淀 B.过滤 C.煮沸 D.蒸馏 E.吸附
(2)自来水厂常用二氧化氯进行消毒,二氧化氮的化学式为ClO2,该物质中氯元素的化合价为+4
(3)铁制品容易被腐蚀,被生锈的条件是与空气、水接触
(4)当KNO3固体中混有少量NaCl,提纯KNO3的方法是制成较高温度时的饱和溶液,然后降温结晶、过滤..
分析 (1)根据自来水净化水过程中常用的方法分析判断;
(2)根据化学式的写法和化合价原则求出元素的化合价;
(3)根据铁生锈的条件分析回答;
(4)根据混合物的特点分析分离提纯的方法.
解答 解:(1)自来水净化水过程中,使用的净水方法常有沉淀、过滤和吸附等,不适用煮沸和蒸馏的方法.
(2)自来水厂常用二氧化氯进行消毒,二氧化氮的化学式为:ClO2,由于氧显-2价,可以推出该物质中氯元素的化合价为+4.
(3)铁制品容易被腐蚀,被生锈的条件是与空气、水接触;
(4)当KNO3固体中混有少量NaCl,由于KNO3的溶解度受温度的影响比较大,NaCl的溶解度受温度的影响变化不大,所以提纯KNO3的方法是制成较高温度时的饱和溶液,然后降温结晶,过滤.
故答为:(1)CD.(2)ClO2,+4.(3)空气、水接触.(4)制成较高温度时的饱和溶液,然后降温结晶、过滤.
点评 本题考查了净水的知识,完成此题,可以依据已有的知识进行解答,属于基础知识,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.将下列物质分别加入水中,不能形成溶液的是( )
| A. | 冰块 | B. | 蔗糖 | C. | 干冰 | D. | 酒精 |
9.下列实验设计,能达到实验目的是C
| 选项 | 实验目的 | 实验设计 |
| A | 检验CO2 | 燃烧的木条伸入集气瓶内 |
| B | 比较金属镁和铝的活动性 | 将镁条和铝粉分别放入等质量、等浓度的盐酸中 |
| C | 除去氯化钾中的少量氯酸钾 | 加热至不再产生气体 |
| D | 鉴别硬水和软水 | 取等量样品,分别加入等量的肥皂水,振荡 |
13.某化学反应的微观示意图如图,下列关于该反应的说法错误的是( )
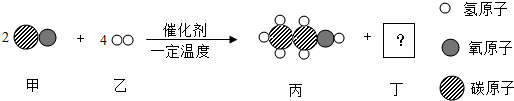

| A. | 丁的化学式为H2O2 | B. | 丙中C、H、O的质量比为12:3:8 | ||
| C. | 甲有毒性 | D. | 该反应不属于置换反应 |
14.下列选项中按单质、化合物、混合物的顺序排列物质的是( )
| A. | 水、加碘食盐、干冰 | B. | 氢气、硫酸钠、液态氧 | ||
| C. | 氮气、小苏打、空气 | D. | 金刚石、大理石、石油 |
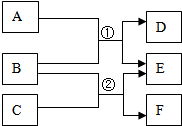 A-F表示初中化学常见的物质,A和B,B和C都能发生反应,且都只能生成两种产物,它们之间的转化关系如图所示.
A-F表示初中化学常见的物质,A和B,B和C都能发生反应,且都只能生成两种产物,它们之间的转化关系如图所示.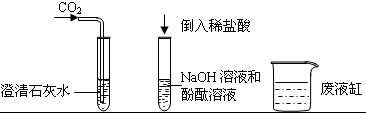
 (
( 表示氧原子;
表示氧原子; 表示氢原子;
表示氢原子; 表示氯原子)
表示氯原子)