题目内容
把氧化铜和铁粉的混合物加到一定量的盐酸中,搅拌充分反应后,过滤.取滤液加入少量铁粉,无任何现象.则下列判断正确的是( )
| A、滤渣可能是铜和铁的混合物 |
| B、滤渣中一定不含铁 |
| C、滤液中含FeCl2和CuCl2 |
| D、滤液中含FeCl2和HCl |
考点:金属的化学性质,酸的化学性质
专题:金属与金属材料
分析:氧化铜和铁粉与盐酸发生反应生成氯化铜和氯化亚铁混合盐溶液.若溶液中同时存在这两种盐,加入铁粉时铁会置换氯化铜中的铜,从而出现红色物质.
解答:解:由题意可知,加入铁粉没有任何现象,说明盐酸不过量,已经全部反应完;氧化铜和铁粉与盐酸发生反应生成氯化铜和氯化亚铁混合盐溶液,若溶液中同时存在这两种盐,加入铁粉时铁会置换氯化铜中的铜,从而出现红色物质.但从题目中我们可以看出没有出现任何现象,说明溶液中不可能同时有这两种盐.
A、氧化铜与稀盐酸反应生成了氯化铜,氯化铜与铁反应生成的单质铜,所以滤渣中一定含铜.铁可能剩余,故A答案正确;
B、由A分析可知,滤渣中一定含有铜,可能含有铁,铁过量时滤渣中就含有铁,故B答案错误;
C、滤液中若含有FeCl2和CuCl2,那么加入铁粉应有红色固体析出.故C答案不正确;
D、因为加入铁粉没有气泡冒出,就说明没有HCl,故D答案不正确.
故选A.
A、氧化铜与稀盐酸反应生成了氯化铜,氯化铜与铁反应生成的单质铜,所以滤渣中一定含铜.铁可能剩余,故A答案正确;
B、由A分析可知,滤渣中一定含有铜,可能含有铁,铁过量时滤渣中就含有铁,故B答案错误;
C、滤液中若含有FeCl2和CuCl2,那么加入铁粉应有红色固体析出.故C答案不正确;
D、因为加入铁粉没有气泡冒出,就说明没有HCl,故D答案不正确.
故选A.
点评:本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
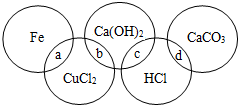 铁、氯化铜、石灰水、稀盐酸、石灰石之间的反应关系如图所示,图中两圆相交部分(a、b、c、d)表示物质间反应的类型或主要实验现象.下列说法中错误的是( )
铁、氯化铜、石灰水、稀盐酸、石灰石之间的反应关系如图所示,图中两圆相交部分(a、b、c、d)表示物质间反应的类型或主要实验现象.下列说法中错误的是( )| A、a处产生红色物质 |
| B、b处生成蓝色沉淀 |
| C、c处发生复分解反应 |
| D、d处生成白色沉淀 |
酚酞是常用的酸碱指示剂,分子式为C20H14O4.下列关于酚酞的说法正确的是( )
| A、酚酞遇盐酸显红色 |
| B、酚酞是由碳、氢、氧三种元素组成的 |
| C、酚酞中碳、氢、氧三种元素的质量比为20:14:4 |
| D、酚酞是由20个碳原子、14个氢原子和4个氧原子构成的 |
过氧化氢(H2O2)具有广泛用途,医疗上可用于清理伤口,实验室可用于制取氧气等.下列有关叙述中错误的是( )
| A、过氧化氢是纯净物 |
B、过氧化氢的微观模型可表示为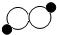 |
| C、过氧化氢是由两个氢原子和两个氧原子构成的 |
| D、过氧化氢中氢元素和氧元素的质量比为1:16 |
氧气的化学性质比较活泼,能与多种物质反应.下列关于氧气的说法正确的是( )
| A、许多物质都能在氧气中燃烧说明氧气具有可燃性 |
| B、鱼虾等能在水中生存是由于氧气极易溶于水 |
| C、铁、硫、酒精在氧气中燃烧都是化合反应 |
| D、氧气与铝常温下反应生成致密的氧化膜 |
下列离子组能在pH=1的无色溶液中大量共存的是( )
| A、NO3- Fe3+ Na+ OH- |
| B、K+ SO42- Na+ NO3- |
| C、Cl- K+ SO42- Ba2+ |
| D、Ca2+ Cl- CO32- Na+ |