题目内容
4.如图所示对两幅微观示意图揭示了化学变化的微观实质.相关说法中正确的是( )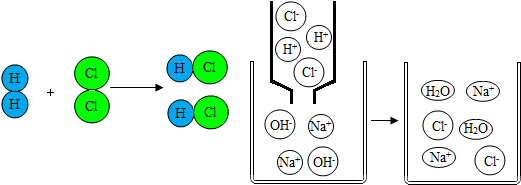
| A. | 在化学变化中物质的质量是守恒的 | |
| B. | 原子在化学变化中是可以再分的 | |
| C. | 两幅图表示的都是化合反应 | |
| D. | 以上图示中涉及的物质都属于化合物 |
分析 这两幅图表示了微观的化学反应过程,说明化学变化的实质就是分子分成原子,原子再重新组合的过程,在反应前后,原子的种类和数目都不变,在溶液中,主要是离子参加反应,有些离子不参加反应,反应前后种类和数目保持不变.
解答 解:A、由于反应前后原子的种类和数目都不变,所以,在化学变化中物质的质量是守恒的,故A正确;
B、原子在化学变化中不能再分,只是重新组合,B错误;
C、由反应的特点可知,第一幅表示的是化合反应,第二幅表示复分解反应,故C错误;
D、由物质的微观构成可知,氢气和氯气属于单质,不是化合物,故D错误.
故选:A.
点评 要求同学们能看懂化学反应的模拟图形,能从分子、原子的观点分析化学变化的实质.此题对这部分知识点有很好的练习作用.

练习册系列答案
相关题目
14.小明同学所做的下列课外小实验中,主要发生化学变化的是( )
| A. | 自制白糖晶体 | B. | 用白醋和蛋壳制二氧化碳 | ||
| C. | 自制简易净水器 | D. | 用石墨做导电实验 |
12.下列实验现象描述正确的是( )
| A. | 硫在氧气中燃烧产生淡蓝色火焰 | |
| B. | 细铁丝在空气中燃烧,火星四射,生成黑色固体 | |
| C. | 向滴有酚酞的氢氧化钠溶液中,通入足量的二氧化碳,溶液会由红色变为无色 | |
| D. | 红磷在氧气中燃烧能产生大量的白烟 |
19.某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液加入稀盐酸一会后,发现忘记了滴加指示剂.因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究.
Ⅰ、写出该中和反应的化学方程式Ca(OH)2+2HCl=CaCl2+2H2O.
Ⅱ、探究烧杯内溶液中溶质的成分.
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】猜想一:可能是CaCl2和Ca(OH)2;猜想二:可能只有CaCl2;猜想三:可能是CaCl2和HCl
【查阅资料】氯化钙溶液呈中性.
【进行实验】
【反思与拓展】
( 1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量.
(2)烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是溶液呈酸性,腐蚀管道或造成水污染.要处理烧杯内溶液,使其溶质只含有CaCl2,应向烧杯中加入过量的石灰石.
Ⅰ、写出该中和反应的化学方程式Ca(OH)2+2HCl=CaCl2+2H2O.
Ⅱ、探究烧杯内溶液中溶质的成分.
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】猜想一:可能是CaCl2和Ca(OH)2;猜想二:可能只有CaCl2;猜想三:可能是CaCl2和HCl
【查阅资料】氯化钙溶液呈中性.
【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡 | 溶液无明显变化或溶液不变红色 | 猜想一不正确 |
| 另取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量 | 先有气体产生,后产生沉淀 | 猜想二不正确 猜想三正确 |
( 1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量.
(2)烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是溶液呈酸性,腐蚀管道或造成水污染.要处理烧杯内溶液,使其溶质只含有CaCl2,应向烧杯中加入过量的石灰石.
9.下列实验操作的方法中正确的是( )
| A. | 给试管加热之前要先预热 | |
| B. | 用50 mL的量筒量取5.55 mL的氯化钠溶液 | |
| C. | 将氢氧化钠固体直接放在托盘天平的托盘上称量 | |
| D. | 用pH试纸直接浸入溶液中测溶液的pH |
13.某科学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用8g石灰石样品,把100g稀盐酸分为4次加入样品中(杂质既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下:
(1)从以上数据可知,这四次实验中,第3、4次实验反应后盐酸有剩余.
(2)表中m=3;n=1.2.
(3)求石灰石样品中碳酸钙的质量分数.
(4)求实验室所用稀盐酸的溶质质量分数.
| 序号 | 加入稀盐酸的质量(g) | 剩余固体的质量(g) |
| 1 | 25 | 5.5 |
| 2 | 25 | m |
| 3 | 25 | 1.2 |
| 4 | 25 | n |
(2)表中m=3;n=1.2.
(3)求石灰石样品中碳酸钙的质量分数.
(4)求实验室所用稀盐酸的溶质质量分数.
 2015年3月22日是第23届“世界水日”,节约水资源,保护水安全是每个公民的义务和责任.
2015年3月22日是第23届“世界水日”,节约水资源,保护水安全是每个公民的义务和责任.