题目内容
11.酗酒对人体健康的危害很大,因为饮下白酒约5分钟后,酒精就会进入血液,随血液在全身流动,人的组织器官和各个系统都要受到酒精的毒害.酒精,又名乙醇,它的化学式为C2H5OH.求:(要求写出解题格式)(1)乙醇的相对分子质量.
(2)乙醇中碳元素的质量分数.
(3)92克乙醇中碳元素的质量为多少克.
分析 (1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)乙醇的相对分子质量为:12×2+1×5+16×5=46.
(2)乙醇中碳元素的质量分数为$\frac{12×2}{46}$×100%≈52.2%.
(3)92克乙醇中碳元素的质量为92g×$\frac{12×2}{46}$×100%=48g.
答:(1)乙醇的相对分子质量为46;
(2)乙醇中碳元素的质量分数为52.2%;
(3)92克乙醇中碳元素的质量为48g.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
2.在制取CO2的实验中,小科发现质量相同而粗细不同的大理石与盐酸反应,CO2的产生速度细的比粗的快得多.经思考后,小科设计了如下实验(每次实验均用1g大理石,20mL盐酸)
(1)为了比较反应速度,设计如图一所示装置,其中量筒的作用是通过观察单位时间内排入量筒中水的体积来判断反应速率;
(2)实验中CO2体积随时间的变化关系如图二所示,请将实验2中CO2体积随时间变化的曲线画在图二中.
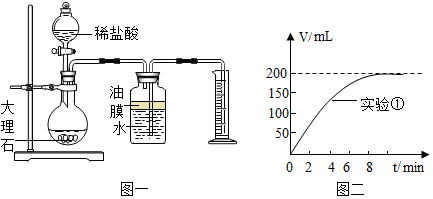
(3)已知20℃该气压下CO2气体密度约1.98g/L,求大理石中CaCO3的质量分数?(详细计算过程)(C-12 O-16 Ca-40)
| 实验序号 | 温度(℃) | 大理石颗粒 | 盐酸质量分数(%) | 实验目的 |
| 1 | 20 | 粗 | 5 | 探究大理石和盐酸的反应速度与石灰石颗粒大小的关系 |
| 2 | 20 | 细 | 5 |
(2)实验中CO2体积随时间的变化关系如图二所示,请将实验2中CO2体积随时间变化的曲线画在图二中.

(3)已知20℃该气压下CO2气体密度约1.98g/L,求大理石中CaCO3的质量分数?(详细计算过程)(C-12 O-16 Ca-40)
6.NH3和Cl2混合可发生下列化学反应:2NH3+3Cl2=6HCl+N2,该反应的基本类型是( )
| A. | 化合反应 | B. | 分解反应 | C. | 复分解反应 | D. | 置换反应 |
3.20℃时,将30克某物质投入到50克水中充分溶解,还有10克未溶解,问20℃时,该物质的溶解度为( )
| A. | 50克 | B. | 30克 | C. | 40 | D. | 40克 |
20.金属钴(Co)与铁的化学性质相似,都能与稀盐酸反应,在化合物中钴元素常显+2,+3价,下列说法正确的是( )
| A. | CoCl3读作“氯化亚钴” | |
| B. | 补充钴元素可以防止贫血 | |
| C. | 金属铜不能与CoCl2溶液发生反应 | |
| D. | CoCl2中钴元素的质量分数约为33.3% |
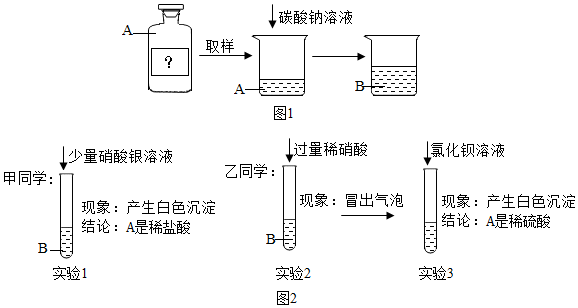
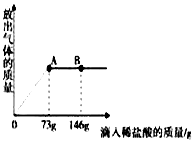 在一烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,加入109.1g水溶解,制成溶液.向其中滴加溶质质量分数10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系如图所示,请回答问题:
在一烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,加入109.1g水溶解,制成溶液.向其中滴加溶质质量分数10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系如图所示,请回答问题: