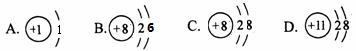题目内容
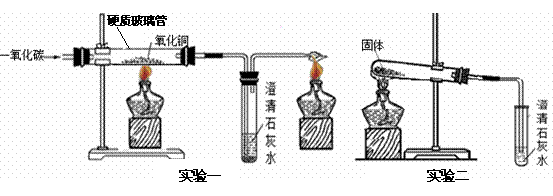 下面是一氧化碳和碳粉分别还原氧化铜的实验:
下面是一氧化碳和碳粉分别还原氧化铜的实验:
(1)实验一:
①硬质玻璃管中反应的化学方程式 ;
②小鱼质疑,应在装置左端连接一个装有澄清石灰水的试管,以便验证一氧化碳能否使澄清石灰水变浑浊。同学们讨论了该实验的步骤后,都觉得无此必要,请你说明其中理由
。
(2)实验二:要保证该实验成功,有以下关键环节:
①较高的温度。据此,实验中应对酒精灯进行的改进是 。
②两种固体反应物的质量比。若碳不足,则氧化铜不能被全部还原;若碳过多,则除了生成铜和二氧化碳外还会生成 (填化学式)。
(3)若两实验中,氧化铜都反应完全,且都只生成二氧化碳。
实验数据记录如下:
| 反应前 | 反应后 | |
| 实验一,硬质玻璃管+固体的质量 | 142g | 140.4g |
| 实验二,试管+固体的质量 | 184g | 181.8g |
根据以上数据,计算“实验一”中生成二氧化碳 g,“实验二”中生成铜 g。
(1)① CO+ CuO  Cu + CO2
Cu + CO2
②点燃酒精灯之前需先通入一氧化碳排尽装置中的空气,一氧化碳已经与石灰水接触,未见浑浊
(2)① 加一网罩 (灯罩) ② CO
(3) 4.4 g 6.4 g

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案通过一个月的化学学习,应该 知道有多种途径可以制取氧气。如:
知道有多种途径可以制取氧气。如:
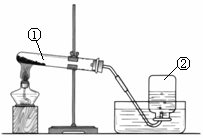 A.电解水 B.分离空气
A.电解水 B.分离空气
C.加热高锰酸钾 D.分解过氧化氢
E.
(1)请在E处写出另一种制取氧气的文字反应式;
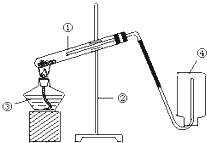
(2)若用右图装置加热高锰酸钾制取氧气,实验结束,停止加热时要先把导管移出水面,其理由是 ,此时发现水槽中的水变成了浅紫红色,你认为产生该现象的原因可能是 ;
(3)若分解过氧化氢制取氧气,供选用的装置如下:

 | |||||||
 | |||||||
|
| ||||||
要得到平稳的氧气流,应选用的发生装置 是 (选填“甲”或“乙”);
是 (选填“甲”或“乙”);
若用丙装置收集生成的氧气, 气体应从
气体应从  (选填“a”或“b”)端导入。
(选填“a”或“b”)端导入。
物质的下列性质,属于化学性质的是( )
|
| A. | 颜色、状态 | B. | 密度、硬度 | C. | 氧化性、可燃性 | D. | 熔点、沸点 |
用酒精灯给试管里的液体加热时,发现试管破裂,可能有的原因有:①用酒精灯的外焰给试管加热;②加热前没有擦干试管外壁的水;③加热时试管底部触及灯芯;④被加热的液体超过试管容积的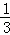 ;⑤没有进行预热.其中与之有关的是( )
;⑤没有进行预热.其中与之有关的是( )
|
| A. | ①③⑤ | B. | ②④ | C. | ②③⑤ | D. | ③④⑤ |