题目内容
13.空气是人类宝贵的自然资源.下列有关空气的说法正确的是( )| A. | 空气中的氧气约占空气总体积的五分之四 | |
| B. | 二氧化碳是造成酸雨的主要物质 | |
| C. | 空气中的稀有气体不与任何物质发生反应 | |
| D. | 空气中的氮气可作为生产氮肥的原料 |
分析 空气中各成分的体积分数分别是:氮气大约占78%、氧气大约占21%、稀有气体大约占0.94%、二氧化碳大约占0.03%、水蒸气和其它气体和杂质大约占0.03%;空气的成分主要以氮气和氧气为主,氧气约占五分之一,氮气约占五分之四.氮气的用途是:制造氮肥、氮气充入食品包装袋内可以防腐、液态氮可以做制冷剂.
解答 解:A、空气中的氧气约占空气总体积的五分之一,不是五分之四,故选项错误;
B、二氧化硫是造成酸雨的主要物质,故选项错误;
C、空气中的稀有气体不与任何物质发生反应错误,一定条件下也会反应,故选项错误;
D、氮气的用途是:制造氮肥、氮气充入食品包装袋内可以防腐、液态氮可以做制冷剂,故选项正确;
故选D
点评 本考点考查了空气中各种气体的含量和用途等,同学们要加强记忆有关的知识点,在理解的基础上加以应用,本考点基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.现有一定量的硫酸铜和硫酸的混合溶液,为测定其中硫酸铜的质量,将其让如烧杯中,然后用一溶质质量分数的氢氧化钠溶液120g平均分六次加入其中,充分振荡后,实验所得数据见下表,请你分析并进行有关计算:
(1)上表中X的数值为4.90g;
(2)原混合溶液中硫酸铜的质量;
(3)所用氢氧化钠溶液的质量分数.
| 1 | 2 | 3 | 4 | 5 | 6 | |
| 加入氢氧化钠溶液的质量/g | 20 | 20 | 20 | 20 | 20 | 20 |
| 生成沉淀的质量/g | 0 | 2.45 | X | 7.35 | 9.8 | 9.8 |
(2)原混合溶液中硫酸铜的质量;
(3)所用氢氧化钠溶液的质量分数.
18.某校实验小组在做“盐酸中和氢氧化钠溶液”的实验,一同学滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度.于是他们对所得溶液的酸碱性进行探究.
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈碱性,也可能呈酸性,还可能呈中性.
【实验验证】
【分析与思考】
(1)若溶液呈碱性,为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入FeCl3(填化学式,合理均可)溶液,能观察到产生沉淀,沉淀的化学式为Fe(OH)3;等到不再产生沉淀为止,过滤混合溶液,把滤液倒入蒸发皿中加热,还可得到氯化钠晶体.
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入碳酸钠溶液,若观察到有气泡冒出,则所取溶液呈酸性;若无明显现象,则呈中性.
方案二:取样,加入金属锌,若有所泡产生,则所取溶液呈酸性,该反应的化学方程式为Zn+2HCl═ZnCl2+H2↑;若无明显现象,则呈中性.
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈碱性,也可能呈酸性,还可能呈中性.
【实验验证】
| 实验操作 | 实验现象 | 结论 |
| 用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡 | 无色酚酞试液变红 | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈酸性或中性 |
(1)若溶液呈碱性,为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入FeCl3(填化学式,合理均可)溶液,能观察到产生沉淀,沉淀的化学式为Fe(OH)3;等到不再产生沉淀为止,过滤混合溶液,把滤液倒入蒸发皿中加热,还可得到氯化钠晶体.
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入碳酸钠溶液,若观察到有气泡冒出,则所取溶液呈酸性;若无明显现象,则呈中性.
方案二:取样,加入金属锌,若有所泡产生,则所取溶液呈酸性,该反应的化学方程式为Zn+2HCl═ZnCl2+H2↑;若无明显现象,则呈中性.
3.工业用盐中含有的亚硝酸钠(NaNO2)是一种有毒物质,利用 NH4Cl溶液可使NaNO2转化为无毒物质.该反应分两步进行:①NaNO2+NH4Cl═NaCl+NH4NO2②NH4NO2═N2↑+2H2O
下列叙述不正确的是( )
下列叙述不正确的是( )
| A. | NH4NO2由三种元素组成 | |
| B. | 反应①为复分解反应,反应②为分解反应 | |
| C. | 利用 NH4Cl 处理NaNO2最终转化为NaCl、N2和H2O | |
| D. | 上述反应所涉及的物质中,氮元素的化合价有四种 |
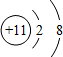 表示的微粒符号为Na+.
表示的微粒符号为Na+.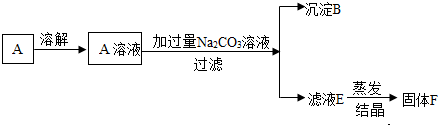
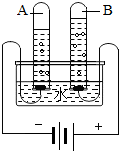 如图是电解水的实验简图,若A试管中产生10mL气体,则B试管中产生5mL气体.
如图是电解水的实验简图,若A试管中产生10mL气体,则B试管中产生5mL气体.