题目内容
1.某化学兴趣小组围绕“酸和碱反应”的学习,进行了如图甲、乙所示的两个探究实验: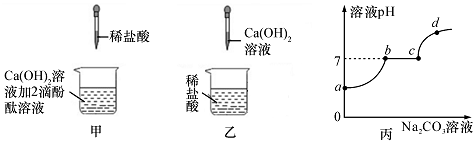
(1)在进行甲实验时,判断反应恰好完全的实验依据是B.
A.溶液中的OH-离子刚好与加入的H+完全结合
B.溶液的颜色刚好变为无色
C.溶液的颜色刚好变为蓝色
D.溶液的pH刚好等于7
(2)取实验乙反应后的溶液逐滴滴加Na2CO3溶液,并用pH计测出溶液的pH值,溶液的pH变化如图丙所示.由图可知,在未加入Na2CO3溶液前,在反应后的溶液中滴加紫色石蕊试液,溶液呈红色.
(3)图丙中,ab段发生的反应的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑,c点溶液中所含的溶质是NaCl(填化学式).
分析 氢氧化钙溶液显碱性,能使酚酞试液变红色,能和稀盐酸反应生成氯化钙和水,氯化钙溶液显中性,不能使酚酞试液变色;
碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,和氯化钙反应生成碳酸钙沉淀和氯化钠.
解答 解:(1)在进行甲实验时,判断反应恰好完全的实验依据是溶液的颜色刚好变为无色.
故填:B.
(2)由图可知,在未加入Na2CO3溶液前,溶液pH小于7,溶液显酸性,能使石蕊试液变红色.
故填:红.
(3)图丙中,ab段碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,发生的反应的化学方程式是:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
c点时碳酸钠和氯化钙恰好完全反应,因此溶液中所含的溶质是NaCl.
故填:Na2CO3+2HCl═2NaCl+H2O+CO2↑;NaCl.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
12.在不用指示剂的条件下,将含有盐酸的氯化钙溶液由酸性变为中性,应选用( )
| A. | 澄清石灰水 | B. | 硝酸银溶液 | C. | 石灰石 | D. | 生石灰粉末 |
9.下列四种变化中,其中一种与其它三者有本质的区别,它应该是( )
| A. | 铁生锈 | B. | 水汽化 | C. | 煤燃烧 | D. | 苹果腐烂 |
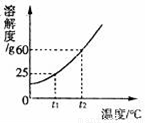
10. 在20℃时,在两只各盛有100克水的烧杯中,分别加入60克氯化钠和蔗糖固体,搅拌使其充分溶解,结果如图所示.下列说法正确的是( )
在20℃时,在两只各盛有100克水的烧杯中,分别加入60克氯化钠和蔗糖固体,搅拌使其充分溶解,结果如图所示.下列说法正确的是( )
 在20℃时,在两只各盛有100克水的烧杯中,分别加入60克氯化钠和蔗糖固体,搅拌使其充分溶解,结果如图所示.下列说法正确的是( )
在20℃时,在两只各盛有100克水的烧杯中,分别加入60克氯化钠和蔗糖固体,搅拌使其充分溶解,结果如图所示.下列说法正确的是( )| A. | 两烧杯中的溶液质量相等 | |
| B. | 20℃时两者的溶解度相等 | |
| C. | 蔗糖溶液一定刚好是饱和溶液 | |
| D. | 氯化钠溶液的浓度一定比蔗糖溶液小 |
11.小红同学向盐酸与氯化钡的混合溶液中逐滴滴入碳酸钠溶液至过量,记录滴入的碳酸钠溶液的质量(x)与有关量的变化关系如图所示,下列判断正确的是( )
| A. | 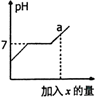 当碳酸钠溶液加至a点时,溶液中Na2CO3正与BaCl2发生反应 当碳酸钠溶液加至a点时,溶液中Na2CO3正与BaCl2发生反应 | |
| B. |  当碳酸钠溶液加至b点时,所得溶液的pH=7 当碳酸钠溶液加至b点时,所得溶液的pH=7 | |
| C. | 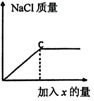 当碳酸钠溶液加至c点时,溶液中含有的溶质是氯化钠和氯化钡 当碳酸钠溶液加至c点时,溶液中含有的溶质是氯化钠和氯化钡 | |
| D. |  当碳酸钠溶液加至d点时,溶液中BaCl2与Na2CO3恰好反应完全 当碳酸钠溶液加至d点时,溶液中BaCl2与Na2CO3恰好反应完全 |
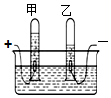 如图是实验室电解水的简易装置示意图,回答下列问题:
如图是实验室电解水的简易装置示意图,回答下列问题: