题目内容
17.下列各组物质可按溶解、过滤、蒸发的操作顺序分离的是( )| A. | 氯化钾和碳酸钙 | B. | 硝酸钾和硝酸钠 | C. | 氧化铜和炭粉 | D. | 水和植物油 |
分析 按照“溶解、过滤、蒸发”的步骤进行分离的物质,必须需要满足两种固体物质的溶解性不同,必须具备:一种不能溶于水,另一种物质能溶于水.
解答 解:A、氯化钾溶于水,而碳酸钙不溶于水,能按溶解、过滤、蒸发的操作顺序分离,故选项正确.
B、硝酸钾和硝酸钠均易溶于水,不能按溶解、过滤、蒸发的操作顺序分离,故选项错误.
C、氧化铜和炭粉均难溶于水,不能按溶解、过滤、蒸发的操作顺序分离,故选项错误.
D、植物油难溶于水,但是液体,不能按溶解、过滤、蒸发的操作顺序分离,故选项错误.
故选:A.
点评 本题考查了混合物的分离,理解过滤的原理(是将不溶于液体的固体分离的方法)、掌握常见物质的溶解性是正确解答此类题的关键.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案
相关题目
8.用砂纸打磨过的镁条与稀盐酸反应时,现象为:反应剧烈,产生大量气泡,且试管明显发热,但是,在分组实验中,部分小组除观察到上述现象外还看到:出现白色不溶物.
【提出问题】分组试验中,为什么有的小组出现白色不溶物?
【实验探究一】在4支试管中加入等量、同浓度的稀盐酸,加入宽窄相同、用砂纸打磨过的镁条,反应后静置观察,结果如下表:
【实验结论】出现白色不溶物是因为镁条用量过多.
【提出问题二】分组实验中,出现的白色不溶物是什么?
【查阅资料】
①在MgCl2溶液中,MgCl2能发生微弱水解,反应为:MgCl2+2H2O=Mg(OH)2+2HCl或MgCl2+H2O=Mg(OH)Cl+HCl;加热能促进水解反应的进行.
②AgNO3与可溶性氯化物在溶液中可发生复分解反应生成不溶于稀硝酸的白色沉淀AgCl,该性质可以用来检验溶液中是否含有氯化物.
③Mg(OH)2和Mg(OH)Cl均为白色固体,不溶于水,能与盐酸、硝酸等反应.
【猜想与假设】
Ⅰ.反应过程中镁有剩余;Ⅱ.镁用量增多使生成的MgCl2增多而析出晶体
Ⅲ.生成了Mg(OH)2白色沉淀;Ⅳ.生成了Mg(OH)Cl白色沉淀
【实验探究二】过滤【实验探究一】D试管中的物质,将得到的白色不溶物分成三份,进行实验:
(1)取第一份白色不溶物于试管中,加入稀盐酸,现象为没有气泡产生.
结论:假设Ⅰ不成立.
(2)取第二份白色不溶物于试管中,加入适量蒸馏水,充分振荡后,不溶物没有减少.
结论:假设Ⅱ不成立.
(3)取第三份白色不溶物于试管中,加入适量稀硝酸,发现不溶物立即溶解,向所得无色溶液中加入几滴硝酸银溶液,出现白色沉淀.
结论:白色不溶物中一定含有氯元素,由此推出假设Ⅳ一定成立(填“一定不”、“一定”或“可能”,下同),假设Ⅲ一定不成立.
【实验反思】
(1)甲同学对上述实验(3)的结论提出疑问,他认为实验(3)的设计不严密,要验证假设Ⅳ是否成立,在进行实验(3)之前应该排除溶液中氯离子的干扰.
(2)在老师的帮助下,实验小组最终确定白色不溶物为Mg(OH)Cl,试写出镁与盐酸反应生成Mg(OH)Cl的化学反应方程式2Mg+3HCl+H2O=Mg(OH)Cl+2H2↑;为避免镁与盐酸反应生成Mg(OH)Cl,请你提出一条合理化建议使用足量的酸.
【提出问题】分组试验中,为什么有的小组出现白色不溶物?
【实验探究一】在4支试管中加入等量、同浓度的稀盐酸,加入宽窄相同、用砂纸打磨过的镁条,反应后静置观察,结果如下表:
| 试管 | A | B | C | D |
| 镁条长度 | 1cm | 2cm | 3cm | 4cm |
| 不溶物 | 无 | 少量 | 较多 | 很多 |
【提出问题二】分组实验中,出现的白色不溶物是什么?
【查阅资料】
①在MgCl2溶液中,MgCl2能发生微弱水解,反应为:MgCl2+2H2O=Mg(OH)2+2HCl或MgCl2+H2O=Mg(OH)Cl+HCl;加热能促进水解反应的进行.
②AgNO3与可溶性氯化物在溶液中可发生复分解反应生成不溶于稀硝酸的白色沉淀AgCl,该性质可以用来检验溶液中是否含有氯化物.
③Mg(OH)2和Mg(OH)Cl均为白色固体,不溶于水,能与盐酸、硝酸等反应.
【猜想与假设】
Ⅰ.反应过程中镁有剩余;Ⅱ.镁用量增多使生成的MgCl2增多而析出晶体
Ⅲ.生成了Mg(OH)2白色沉淀;Ⅳ.生成了Mg(OH)Cl白色沉淀
【实验探究二】过滤【实验探究一】D试管中的物质,将得到的白色不溶物分成三份,进行实验:
(1)取第一份白色不溶物于试管中,加入稀盐酸,现象为没有气泡产生.
结论:假设Ⅰ不成立.
(2)取第二份白色不溶物于试管中,加入适量蒸馏水,充分振荡后,不溶物没有减少.
结论:假设Ⅱ不成立.
(3)取第三份白色不溶物于试管中,加入适量稀硝酸,发现不溶物立即溶解,向所得无色溶液中加入几滴硝酸银溶液,出现白色沉淀.
结论:白色不溶物中一定含有氯元素,由此推出假设Ⅳ一定成立(填“一定不”、“一定”或“可能”,下同),假设Ⅲ一定不成立.
【实验反思】
(1)甲同学对上述实验(3)的结论提出疑问,他认为实验(3)的设计不严密,要验证假设Ⅳ是否成立,在进行实验(3)之前应该排除溶液中氯离子的干扰.
(2)在老师的帮助下,实验小组最终确定白色不溶物为Mg(OH)Cl,试写出镁与盐酸反应生成Mg(OH)Cl的化学反应方程式2Mg+3HCl+H2O=Mg(OH)Cl+2H2↑;为避免镁与盐酸反应生成Mg(OH)Cl,请你提出一条合理化建议使用足量的酸.
5.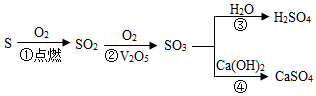 含硫元素物质间发生转化:其中硫元素化合价发生变化的是( )
含硫元素物质间发生转化:其中硫元素化合价发生变化的是( )
 含硫元素物质间发生转化:其中硫元素化合价发生变化的是( )
含硫元素物质间发生转化:其中硫元素化合价发生变化的是( )| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
12.2009年“中国水周”的主题是:“落实科学发展观,节约保护水资源”.下列关于水的说法正确的是( )
| A. | 为了防止水体富营养化应禁止使用含磷洗衣粉 | |
| B. | 通过静置、吸附、过滤、消毒得到的水是纯净物 | |
| C. | 生活中常用煮沸的方法来降低水的硬度 | |
| D. | 水通电可以得到氢气和氧气,说明水中含有氢气和氧气 |
2.“有其他物质生成“是判断物质发生化学变化的依据.但在实际化学反应中,常常根据反应伴随的现象来确定化学反应是否发生.根据你对化学反应的理解填写下表:
| 实验内容 | 主要实验现象 | 化学方程式 |
| 在盛有硝酸银溶液的试管中,插入一根洁净的铜丝 | 铜丝的表面出现银白色物质,溶液变为蓝色 | Cu+2AgNO3═Cu(NO3)2+2Ag |
| 向硝酸银溶液中滴加稀盐酸 | 有白色沉淀生成 | HCl+AgNO3═AgCl↓+HNO3 |
| 将生锈的铁钉放入稀盐酸中 | 铁锈消失,溶液变为黄色 | Fe2O3+6HCl═2FeCl3+3H2O |
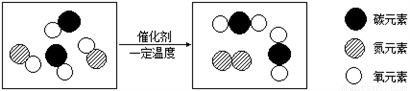
 如图为某学生用高锰酸钾来制取氧气,并用排水法收集的装置图.
如图为某学生用高锰酸钾来制取氧气,并用排水法收集的装置图.