题目内容
16.如图是实验室常用的实验仪器与装置,根据所学知识回答下列问题:
(1)写出图中编号仪器名称:a导管、b水槽
(2)利用上图所示装置,采用以下组合能完成实验室制取气体的是BCD.
A.用①③制取氧气 B.用②⑤制取氧气 C.用②④制取二氧化碳 D.用②⑤制取氢气
(3)小波同学将装置②进行了改进,如图Ⅰ和Ⅱ.改进后的装置与②装置相比,装置Ⅰ的优点是可随时控制反应的发生与停止;装置Ⅱ的优点是节约药品(废物利用、可获得平稳的气流、控制反应的速率等).
(4)实验室若用装置Ⅰ制取二氧化碳,铜网上常放置的药品应为石灰石或大理石.
该方法制取的CO2是不纯净的,为证明该气体中含有多种物质,所用的试剂按序排列分别为无水硫酸铜,硝酸银溶液,澄清石灰水.
(5)小明同学想把制取二氧化碳结束后的废液未经处理直接倒入下水道,可能造成的危害是腐蚀铁制下水管道(写一条)
分析 导管是导入气体的仪器,水槽是盛水的仪器;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.二氧化碳中的水蒸气可以用无水硫酸铜检验,氯化氢气体可以用硝酸银溶液检验,二氧化碳可以用澄清的石灰水检验;实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.装置Ⅰ的优点是:可随时控制反应的发生与停止;装置Ⅱ的优点是:节约药品(废物利用、可获得平稳的气流、控制反应的速率等);小明同学想把制取二氧化碳结束后的废液未经处理直接倒入下水道,可能造成的危害是:腐蚀铁制下水管道.
解答 解:(1)导管是导入气体的仪器,水槽是盛水的仪器,故答案为:导管 水槽
(2)如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集;故答案为:BCD;
(3)装置Ⅰ的优点是:可随时控制反应的发生与停止;装置Ⅱ的优点是:节约药品(废物利用、可获得平稳的气流、控制反应的速率等);故答案为:可随时控制反应的发生与停止;
(4)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳中的水蒸气可以用无水硫酸铜检验,氯化氢气体可以用硝酸银溶液检验,二氧化碳可以用澄清的石灰水检验;故答案为:石灰石或大理石;无水硫酸铜,硝酸银溶液,澄清石灰水;
(5)小明同学想把制取二氧化碳结束后的废液未经处理直接倒入下水道,可能造成的危害是:腐蚀铁制下水管道;故答案为:腐蚀铁制下水管道;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的检验等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| 甲 | 乙 | 丙 | |
| 取用金属混合物的质量/g | 10 | 10 | 20 |
| 取用稀硫酸的质量/g | 100 | 120 | 100 |
| 反应后过滤,得干燥固体的质量/g | 4.4 | 4.4 | 14.4 |
(1)10g金属混合物中含铁粉的质量为5.6g.
(2)计算所用稀硫酸中溶质的质量分数?
(3)计算甲同学所得溶液中溶质的质量分数?(写出计算过程,计算结果精确到0.1%)
| 温 度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |

要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙 ②升高温度 ③降低温度 ④加入水⑤蒸发水后再恢复到原温度 ⑥加入生石灰.
其中措施正确的是D.
A.②④⑥B.③④C.①③⑤⑥D.①②⑤⑥
(2)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量生石灰后得到的溶液(乙溶液),此时溶液中溶质的质量分数乙<甲(填“>”、“<”或“=”).
(3)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH偏小(填“偏大”、“偏小”或“不受影响”).
| 物质 | a | b | c | d |
| 反应前质量 | 6.40 | 3.20 | 4.00 | 0.50 |
| 反应后质量 | x | 2.56 | 7.20 | 0.50 |
| A. | d一定是催化剂 | |
| B. | 表中x为4.64 | |
| C. | c中元素的种类等于a、b两种物质中元素的种类之和 | |
| D. | 若a与b的相对分子质量之比为2:l,则反应中a与b的化学计量数之比为1:2 |
| A. | 用灼烧的方法鉴别羊毛和涤纶 | |
| B. | 用紫色石蕊溶液鉴别CO2和CO气体 | |
| C. | 用酚酞鉴别稀盐酸和氯化钠溶液 | |
| D. | 用水鉴别硝酸铵固体和氢氧化钠固体 |
| A. | 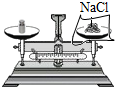 称量NaCl固体 | B. |  稀释浓硫酸 | C. | 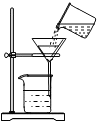 过滤 | D. |  点燃酒精灯 |
| A. | 无色烧碱溶液中滴入酚酞试液变为红色 | |
| B. | 白色硫酸铜粉末遇水蒸气变为蓝色晶体 | |
| C. | 银白色铝片露置在空气中表面逐渐变暗 | |
| D. | 舞台上撒上适量干冰制造出云雾缭绕的景象 |
 实验室一瓶化肥的标签已脱落,只知道它是NH4Cl、(NH4)2SO4、NH4HCO3和尿素[CO(NH2)2]中的一种.请你完成以下探究:
实验室一瓶化肥的标签已脱落,只知道它是NH4Cl、(NH4)2SO4、NH4HCO3和尿素[CO(NH2)2]中的一种.请你完成以下探究: