题目内容
9.家庭日常生活经常用到的下列物质中,属于纯净物的是( )| A. | 食醋 | B. | 白酒 | C. | 铁锅 | D. | 水银 |
分析 根据组成物质的种类,将物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.据此分析物质的类别.
解答 解:A、食醋是醋酸和水的混合物,故选项错误;
B、白酒中有水和酒精等,属于混合物,故选项错误;
C、铁锅一般是铁的合金,合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质,属于混合物,故选项错误;
D、水银是由一种物质组成的,属于纯净物,故选项正确.
故选D.
点评 本考点考查了物质的分类和合金等,与生活实际联系比较密切.要加强记忆混合物、纯净物、单质、化合物、氧化物等基本概念,并能够区分应用.本考点的基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.互为同素异形体的是( )
| A. | 水和过氧化氢 | B. | 铜片和铜丝 | ||
| C. | 金刚石和石墨 | D. | 一氧化碳和二氧化碳 |
18.某市进行理科实验操作考试,其中化学有关于探究金属的某些物理性质和化学性质的试题,用坩埚钳夹取打磨过的铜片在酒精灯上加热,发现铜片表面变黑,为了探究黑色物质的成分.
【查阅资料】(1)铜的氧化物主要有两种:CuO(黑色);Cu2O(红色)
(2)酒精在不完全燃烧使会产生炭黑
(3)炭黑不与稀硫酸反应,也不溶于稀硫酸;氧化铜可与稀硫酸反应而溶解
【提出假设】猜想1:黑色物质为CuO.
猜想2:黑色物质为炭黑
猜想3:黑色物质为CuO与炭黑
【设计方案】
【得出结论】通过实验现象,得出猜想3成立,此黑色固体为混合物,请写出实验中发生的化学方程式CuO+H2SO4=CuSO4+H2O.
【查阅资料】(1)铜的氧化物主要有两种:CuO(黑色);Cu2O(红色)
(2)酒精在不完全燃烧使会产生炭黑
(3)炭黑不与稀硫酸反应,也不溶于稀硫酸;氧化铜可与稀硫酸反应而溶解
【提出假设】猜想1:黑色物质为CuO.
猜想2:黑色物质为炭黑
猜想3:黑色物质为CuO与炭黑
【设计方案】
| 操作步骤 | 实验中可能出现的现象 | 实验结论 |
| 取少量黑色固体于试管中,加入足量稀硫酸(填物质名称) | ①黑色固体消失,溶液变为蓝色 | 猜想1成立 |
| ②黑色固体没有减少,溶液颜色不变 | 猜想2成立 | |
| ③黑色固体部分消失,溶液变蓝 | 猜想3成立 |
19.下列实验操作正确的是( )
| A. | 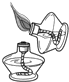 点燃酒精灯 | B. | 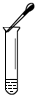 滴加液体 | C. | 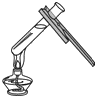 加热液体 | D. | 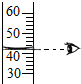 读取液体体积 |

 已知A、B、C、D是初中化学常见的五种物质,均含碳元素.其中,只有A为单质,B和C是含有相同元素的氧化物,D与其它四种物质属于不同的类别,E是大理石的主要成分,它们在一定条件下的转化关系如图所示(反应条件和部分反应物、生成物已省略),请回答:
已知A、B、C、D是初中化学常见的五种物质,均含碳元素.其中,只有A为单质,B和C是含有相同元素的氧化物,D与其它四种物质属于不同的类别,E是大理石的主要成分,它们在一定条件下的转化关系如图所示(反应条件和部分反应物、生成物已省略),请回答: 根据如图回答问题.
根据如图回答问题. 近日网络上出现了“不锈钢水壶中的锰会让人智力低下”等传言,对此,国家食品安全专家钟凯作出了解答.“不锈钢材质中的锰含量与迁移量没有任何必然联系,合金状态下,金属的惰性会增强”,钟凯指出,食品接触材料的重金属迁移量是用强酸、强碱、有机溶剂等,在较高温度下长时间浸泡模拟出来的,如果这种状态下迁移量都没问题,日常使用根本不是问题.
近日网络上出现了“不锈钢水壶中的锰会让人智力低下”等传言,对此,国家食品安全专家钟凯作出了解答.“不锈钢材质中的锰含量与迁移量没有任何必然联系,合金状态下,金属的惰性会增强”,钟凯指出,食品接触材料的重金属迁移量是用强酸、强碱、有机溶剂等,在较高温度下长时间浸泡模拟出来的,如果这种状态下迁移量都没问题,日常使用根本不是问题.