题目内容
10.炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,对实验进行分析并回答: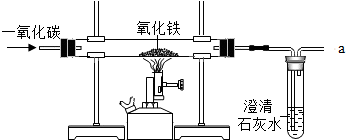
(1)给玻璃管加热的仪器叫酒精喷灯,要用其外焰(填“外焰”、“内焰”或“焰心”)进行加热.
(2)实验中玻璃管里氧化铁粉末的颜色变化是红色粉末变为黑色,观察到试管中的现象是澄清石灰水变浑浊;玻璃管中发生反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)实验前“通入CO”与“开始加热”的顺序是先通入CO后开始加热;实验后“停止通入CO”与“开始加热”的顺序是先开始加热,后停止通入CO;实验后“停止通入CO”与“停止加热”的顺序是先停止加热后停止通入CO.
(4)实验要在装置末端a处燃着一盏酒精灯,其作用是点燃尾气,为了防止一氧化碳对大气的污染.
分析 (1)根据酒精喷灯火焰各部分的温度分析;
(2)根据反应物和生成物,分析实验中玻璃管里氧化铁粉末的颜色变化.根据二氧化碳能与氢氧化钙反应分析澄清石灰水的现象;
(3)根据实验的注意事项进行解答;
(4)根据一氧化碳是对大气有污染的气体分析.
解答 解:(1)由于酒精喷灯的外焰的温度最高,加热时要用外焰进行加热;
(2)由于在高温下,一氧化碳将氧化铁还原为铁,同时生成了二氧化碳.所以实验中玻璃管里氧化铁粉末的颜色变化是红色粉末变黑色;生成的二氧化碳能能使澄清石灰水变浑浊;一氧化碳与氧化铁在高温条件下生成铁和二氧化碳,反应的化学方程式是:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)由于玻璃管内有空气,通入一氧化碳高温时易发生爆炸.所以实验前先通入CO,排净玻璃管中的空气再开始加热,实验后为防止生成的铁被空气中的氧气氧化,所以实验后先开始加热,后停止通入CO;实验后先停止加热后停止通入CO;
(4)为了防止一氧化碳对大气的污染,所以,实验时要在装置末端a处燃着一盏酒精灯除去反应剩余的CO.
故答案为:(1)外焰;
(2)红色粉末变为黑色;澄清石灰水变浑浊;3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)先通入CO后开始加热;先开始加热,后停止通入CO;先停止加热后停止通入CO;
(4)点燃尾气,为了防止一氧化碳对大气的污染.
点评 本题以一氧化碳还原氧化铁为切入点,考查实验中的注意事项、实验现象、反应原理以及环保的问题,考查知识点全面,难度不大.

练习册系列答案
相关题目
1.分类是学习化学的方法之一.下列各组物质是按单质、氧化物、混合物的顺序排列的是( )
| A. | 氮气、高猛酸钾、加碘盐 | B. | 氧气、水、空气 | ||
| C. | 金刚石、干冰、冰水混合物 | D. | 石墨、熟石灰、石油 |
5.将下列物质加入蛋白质试液中,不会使蛋白质失去原有生理活性的是( )
| A. | 甲醛 | B. | 硫酸钠溶液 | C. | 乙酸铅溶液 | D. | 浓硝酸 |
15.2022年北京、张家口将联合举办冬奥会,为办成绿色奥运会,下列措施不可行的是( )
| A. | 将纸质垃圾焚烧处理 | B. | 增加使用太阳能,核能等新能源 | ||
| C. | 废旧电池集中回收处理 | D. | 改进燃煤技术,减少SO2与粉尘排放 |
2.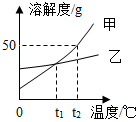 甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
 甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | t1℃时,甲、乙两物质的溶解度相等 | |
| C. | t2℃时,乙的饱和溶液降温至t1℃,乙溶液变为不饱和溶液 | |
| D. | t2℃时,甲物质的饱和溶液降温至t2℃,溶液中溶质质量分数不变 |
20.探究铁冶炼原理实验装置及炼铁高炉的图如下,请据图判断下列叙述中不正确的是( )

| A. | 甲、乙图中得到产物的区别是:甲图完全反应后得到纯净物,而乙得到混合物 | |
| B. | 乙图中高炉炼铁时中原料焦炭的作用是之一是产生热量 | |
| C. | 乙图中生铁出口低于炉渣出口的原因是:铁水密度大于炉渣密度 | |
| D. | 甲图中实验结束时应先停止通一氧化碳再熄灭酒精喷灯 |
