题目内容
8.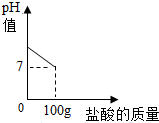 在含氯化钠杂质的纯碱13.6g中逐渐加入质量分数为7.3%稀盐酸,所加稀盐酸的质量关系如图所示:
在含氯化钠杂质的纯碱13.6g中逐渐加入质量分数为7.3%稀盐酸,所加稀盐酸的质量关系如图所示:(1)100g稀盐酸中氯化氢的质量7.3g.
(2)恰好完全反应后,所得溶液中溶质的质量分数?
分析 碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳;由所加稀盐酸的质量关系图,滴加至100g时,前后完全反应,据此由稀盐酸的质量、溶质的质量分数由反应的化学方程式计算出生成氯化钠的质量、参加反应的碳酸钠的质量、生成二氧化碳气体的质量,进而计算出所得溶液中溶质的质量分数即可.
解答 解:(1)100g稀盐酸中氯化氢的质量为100g×7.3%=7.3g.
(2)设反应中碳酸钠、氯化钠、二氧化碳的质量分别为x、y、z,
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 73 117 44
x 7.3g y z
$\frac{106}{73}=\frac{x}{7.3g}$ x=10.6g
$\frac{73}{117}=\frac{7.3g}{y}$ y=11.7g
$\frac{73}{44}=\frac{7.3g}{z}$ z=4.4g
所得溶液的质量分数为$\frac{11.7g+13.6g-10.6g}{13.6g+100g-4.4g}$×100%≈13.5%.
答:(1)7.3g;(2)所得溶液的质量分数为13.5%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,细致地分析图示信息,找出完全反应时消耗的稀盐酸的质量是正确解答本题的前提和关键.

练习册系列答案
相关题目
3.下列实验方案设计不合理的是( )
| A. | 鉴别羊毛和化纤:点燃,是否产生烧焦羽毛气味 | |
| B. | 区分硬水和软水:加入肥皂水 | |
| C. | 检验Na2CO3溶液中含有NaOH:加足量CaCl2 的溶液,过滤,向滤液中滴加酚酞 | |
| D. | 除去Cu中混有的少量CuO:加足量稀硫酸,过滤,洗涤,加热烘干 |
16.化学实验操作直接影响实验结果和人身安全.下列关于实验操作的说法正确的是( )
| A. | 用10mL量筒量取8.55mL水 | |
| B. | 称量固体药品时,左盘放砝码,右盘放物体 | |
| C. | 稀释浓硫酸时,将水沿烧杯内壁注入盛有浓硫酸的烧杯中,并用玻璃棒不断搅拌 | |
| D. | 点燃可燃性气体前必须检验纯度 |
20.下列关于自然界中的水的说法正确的是( )
| A. | 地球上的淡水资源取之不尽,用之不竭 | |
| B. | 水体污染的来源主要有工业污染、农业污染和生活污染 | |
| C. | 水分解可以得到氢气,因此水是廉价且清洁的能源物质 | |
| D. | 水的软化是将海水变成可饮用的淡水 |
17.正确的化学实验操作是实验成功的重要保证.下列实验操作正确的是( )
| A. | 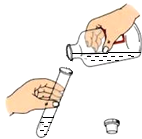 倾倒液体 | B. | 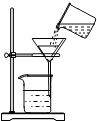 过滤 | ||
| C. |  检查气密性 | D. | 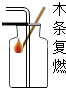 检验氧气是否收集满 |
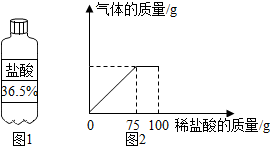 某合作学习小组的同学们.欲测定一定量的某种石灰石样品中碳酸钙的质量,进行了如下实验:
某合作学习小组的同学们.欲测定一定量的某种石灰石样品中碳酸钙的质量,进行了如下实验: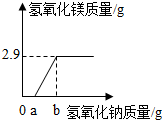 20g硫酸镁溶液中混有少量硫酸,往该溶液中滴加足量氢氧化钠溶液,充分反应后得到2.9g氢氧化镁沉淀.沉淀的质量变化如图所示.
20g硫酸镁溶液中混有少量硫酸,往该溶液中滴加足量氢氧化钠溶液,充分反应后得到2.9g氢氧化镁沉淀.沉淀的质量变化如图所示.