题目内容
1.图是同学们在实验室中进行制取氧气及探究其化学性质的相关实验装置.请回答下列问题:
(1)写出标号①仪器的名称是锥形瓶,固体药品②的名称是二氧化锰
(2)实验室选择A作为制取氧气应选用的发生装置,应该进行的改动是将长颈漏斗换成分液漏斗,写出同学们利用改动后的装置制取氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
(3)可以选择C作为氧气的收集装置,正确连接后可观察到的现象是集气瓶内的水从b被排出
(4)D装置中加入少量水的目的是吸收二氧化硫,防止逸出污染空气
(5)请将用加热KMnO4制取氧气的实验装置图补充完整.
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(3)根据氧气的密度比水的小解答;
(4)根据硫燃烧生成二氧化硫污染空气解答;
(5)根据用加热KMnO4制取氧气的原理及氧气的性质解答.
解答 解:
(1)标号①仪器的名称是锥形瓶;过氧化氢在二氧化锰的催化作用下分解制氧气,不需加热,固体药品②的名称是二氧化锰;
(2)实验室用过氧化氢在二氧化锰的催化作用下制取氧气不需要加热,应选用的发生装置是A装置,为了能够控制反应速率,将长颈漏斗换成分液漏斗;过氧化氢在二氧化锰的催化作用下分解的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)可以选择C作为氧气的收集装置,氧气的密度比水的小,氧气从a进,正确连接后可观察到的现象是集气瓶内的水从b被排出;
(4)硫燃烧生成二氧化硫污染空气,D装置中加入少量水的目的是吸收二氧化硫,防止逸出污染空气;
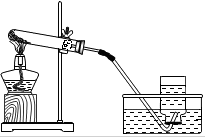
(5)用加热KMnO4制取氧气,为防止高锰酸钾进入导气管,试管口放棉花,图如下: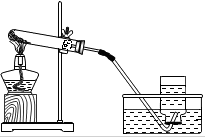
答案:
(1)锥形瓶;二氧化锰;
(2)将长颈漏斗换成分液漏斗;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)集气瓶内的水从b被排出;
(4)吸收二氧化硫,防止逸出污染空气;
(5)
点评 本题考查仪器的用途、装置的选择、化学方程式的书写,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、密度、能否和空气中的物质发生化学反应等因素.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
11.实验室制取气体的装置如图所示,根据所学的知识回答下列问题.
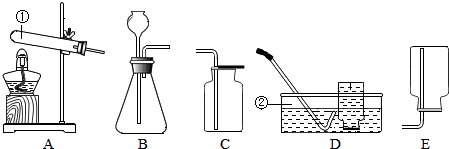
(1)写出图中标有①、②的仪器名称:①试管;②水槽.
(2)若用石灰石和稀盐酸制取二氧化碳,该反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑,应选用的发生装置是B(填标号,下同),收集装置是C,检验CO2是否已经集满的方法是将燃着的木条放在集气瓶口,若木条熄灭,则已集满.AD组合装置可用于制取收集的一种气体是氧气(填物质名称),制取该气体的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
(3)氨气的物理性质及其制取方法 归纳如表.根据表中信息,实验室制取氨气,应采用方法二(填“一”或“二”);据此,应选用的发生装置是A,收集装置是E.

(1)写出图中标有①、②的仪器名称:①试管;②水槽.
(2)若用石灰石和稀盐酸制取二氧化碳,该反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑,应选用的发生装置是B(填标号,下同),收集装置是C,检验CO2是否已经集满的方法是将燃着的木条放在集气瓶口,若木条熄灭,则已集满.AD组合装置可用于制取收集的一种气体是氧气(填物质名称),制取该气体的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
| 物理性质 | 氨气是一种无色有刺激性气味、极易溶于水、密度比空气小的气体 | |
| 制 取 方法 | 方法一 | 氮气与氢气在高温、高压、催化剂的条件下生成氨气 |
| 方法二 | 氯化铵固体与熟石灰粉末在加热条件下生成氨气 | |
12.小明在实验室发现一瓶未知浓度的氢氧化钠溶液,为方便以后使用,他对其浓度进行了测定.取20.0g此氢氧化钠溶液于烧杯中,逐滴滴加溶质质量分数为7.3%的稀盐酸,并随时对反应后的溶液用pH计(一种测定溶液pH的仪器)测定溶液的pH,所得数据如表:
试回答:
(1)当滴加稀盐酸的质量为9.8g时,溶液中的溶质是NaCl、NaOH;当滴加稀盐酸的质量为10.0g时,20.0g该氢氧化钠溶液与稀盐酸恰好完全反应.
(2)计算所测氢氧化钠溶液中溶质的质量分数.
| 加入稀盐酸的质量/g | 9.6 | 9.8 | 9.9 | 10.0 | 10.1 |
| 溶液的pH | 12.4 | 12.1 | 11.8 | 7.0 | 2.2 |
(1)当滴加稀盐酸的质量为9.8g时,溶液中的溶质是NaCl、NaOH;当滴加稀盐酸的质量为10.0g时,20.0g该氢氧化钠溶液与稀盐酸恰好完全反应.
(2)计算所测氢氧化钠溶液中溶质的质量分数.
6.某同学对下列4个实验都设计了两种方案,其中方案一、方案二都合理的是( )
| 选项 | A | B | C | D |
| 实验 目的 | 除去铜粉中少量的铁粉 | 检验某气体为CO2 | 鉴别硫酸钾和硝酸铵两种化肥 | 证明氯化钠溶液和稀盐酸 |
| 方案一 | 用磁铁吸引 | 带火星的木条复燃 | 看外观 | 加紫色石蕊试液 |
| 方案二 | 加稀盐酸 | 加澄清石灰水 | 加熟石灰研磨闻气味 | 加硝酸银溶液 |
| A. | A | B. | B | C. | C | D. | D |
13.“防火胜于救火”,科学认识燃烧,增强安全防范意识是每个公民应具备的安全素养之一. 下列说法错误的是
( )
( )
| A. | 身上着火不可乱跑,要就地打滚使火熄灭 | |
| B. | 水能灭火,是因为水能降低可燃物的着火点 | |
| C. | 对于不明原因引起的失火,我们宁可让其自生自灭,也不能贸然采取灭火措施 | |
| D. | 油库、面粉厂、纺织厂、轮穀厂、橡胶厂和煤矿的坑道内等场所要严禁烟火,以避免爆炸的发生 |
10. 图中是钠元素在元素周期表中的信息和钠原子结构示意图.下列说法错误的是( )
图中是钠元素在元素周期表中的信息和钠原子结构示意图.下列说法错误的是( )
 图中是钠元素在元素周期表中的信息和钠原子结构示意图.下列说法错误的是( )
图中是钠元素在元素周期表中的信息和钠原子结构示意图.下列说法错误的是( )| A. | 钠的原子序数为11 | B. | 钠原子核外有3个电子层 | ||
| C. | 钠的相对原子质量为22.989 | D. | 化学反应中,钠原子易得电子 |
6.“低钠盐”可以控制钠的摄入量从而防治高血压等疾病.制备“低钠盐”是在食盐(NaCl)中按照配方比例添加食用KCl.国内某些生产厂家为改变“低钠盐”口味还会加入少量镁盐(仅限MgSO4或MgCl2).
①测得某“低钠盐”样品a中含有NaCl和KCl的质量分数均为50%.该样品a的水溶液中,含量最多的离子是Cl-(填离子符号).
②探究某“低钠盐”样品b中是否添加镁盐,以及添加的是何种镁盐(MgSO4或MgCl2中的一种).请设计实验方案,完成下列表格.
限选试剂:BaCl2溶液、NaOH溶液、AgNO3溶液、蒸馏水
①测得某“低钠盐”样品a中含有NaCl和KCl的质量分数均为50%.该样品a的水溶液中,含量最多的离子是Cl-(填离子符号).
②探究某“低钠盐”样品b中是否添加镁盐,以及添加的是何种镁盐(MgSO4或MgCl2中的一种).请设计实验方案,完成下列表格.
限选试剂:BaCl2溶液、NaOH溶液、AgNO3溶液、蒸馏水
| 实验操作 | 预期现象级结论 |
| 步骤1:取少量样品b于烧杯中,加足量蒸馏水,并用玻璃棒搅拌 | 样品溶解,形成无色溶液. |
| 步骤2:取少量步骤1形成的溶液于试管中,再滴加少量NaOH溶液,振荡. | 有白色沉淀生成,说明样品b中添加了镁盐. |
| 步骤3:取少量步骤1形成的溶液于试管中,再滴加少量的BaCl2溶液振荡 | 若有白色沉淀产生,则添加的是MgSO4.若无明显现象,则添加的是MgCl2 |
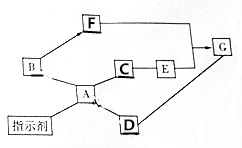 构建知识网络是学习化学的常用方法,A~G都是初中化学中常见的物质,已知A、B、C、D、G是不同类别的物质,A俗称烧碱,D溶液中有蓝色的硫酸盐,B是光合作用的原料,E为红色粉末.它们之间的转化关系如图所示.(图中“-”表示反应,“→”表示转化关系)请回答下列问题:
构建知识网络是学习化学的常用方法,A~G都是初中化学中常见的物质,已知A、B、C、D、G是不同类别的物质,A俗称烧碱,D溶液中有蓝色的硫酸盐,B是光合作用的原料,E为红色粉末.它们之间的转化关系如图所示.(图中“-”表示反应,“→”表示转化关系)请回答下列问题: