题目内容
12.根据已经学习的实验室制取气体的有关知识,请结合如图装置图回答问题:
(1)写出标号仪器的名称:①酒精灯;②锥形瓶.
(2)A是固体制取气体的装置,请改正其中的两处错误:试管口应该略向下倾斜,伸入试管内导管应稍微露出橡皮塞即可.
(3)实验室常用装置B和E组合进行氧气的制取,所发生反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;实验时,若气体产生的速率太快,请写出合理的改进方法调节活塞,减缓液体滴加速度或者向分液漏斗中加水;判断E装置中已经集满氧气的标志是集气瓶口有大气泡冒出.
(4)小刚查阅资料得知,白色固体氯化铵受热分解可以制得氨气和氯化氢气体.于是,小刚想用改正后的A装置加热氯化铵固体制取纯净的氨气,你认为小刚选择的实验药品合理吗?不合理(填“合理”或“不合理”),请你说出合理或不合理的理由因为产生氨气和氯化氢两种气体,不可能得到纯净的氨气.
分析 (1)根据实验室常用仪器解答;
(2)据加热固体的注意事项分析解答;
(3)装置B适用于固体和液体常温反应制取气体,实验室利用过氧化氢制取氧气不需加热,可用此装置;实验时产生气体速度太快,可能是反应物的浓度过大或滴加的速度过快;并据排水法收集气体回答;
(4)氯化铵受热分解可以制得氨气和氯化氢气体,会导致收集的氨气不纯.
解答 解:(1)根据实验室常用仪器可知:①酒精灯;②锥形瓶;
(2)给试管内固体加热时试管口应向下倾斜,防止冷凝水倒流引起试管炸裂,且伸入试管内的导管稍微露出塞子即可,太长不利于气体的导出;
(3)装置B适用于固体和液体常温反应制取气体,实验室利用过氧化氢制取氧气不需加热,可用此装置,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.实验时产生气体速度太快,可能是反应物的浓度过大或滴加的速度过快,所以可调节活塞,减缓液体滴加速度或者向分液漏斗中加水使反应物的浓度降低;利用排水法收集气体时若导管口有气泡冒出,说明收集满了;
(4)氯化铵受热分解可以制得氨气和氯化氢气体,会导致收集的氨气不纯,所以小刚的选择不合理;
故答案为:
(1)①酒精灯;②锥形瓶;
(2)试管口应该略向下倾斜; 伸入试管内导管应稍微露出橡皮塞即可;
(3)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑; 调节活塞,减缓液体滴加速度或者向分液漏斗中加水; 集气瓶口有大气泡冒出;
(4)不合理; 因为产生氨气和氯化氢两种气体,不可能得到纯净的氨气.
点评 本题考查实验装置的选取,化学方程式的书写,考查知识点较多,但难度不大,只要对课本中的基础知识掌握了,就能做好此题.根据装置特点可以判断装置图的正误,根据操作要求可以判断操作是否符合实验室的规定;氧气的验满将带火星的木条放在集气瓶口

| A. | 茶氨酸属于有机高分子化合物 | |
| B. | 一个茶氨酸分子中含有一个氮分子 | |
| C. | 茶氨酸中氧元素的质量分数最大 | |
| D. | 茶氨酸中碳元素与氢元素的质量比为6:1 |
| 名称 | 洗涤灵 | 洁厕灵 | 炉具清洁剂 | 活氧彩漂 | 污渍爆炸盐 |
| 产品样式 |  |  |  |  |  |
| 有效成分或功能 | 清洗油污 | 盐酸 | 氢氧化钠 | 过氧化氢 | 过碳酸钠 |
(2)清除以下物质,可使用炉具清洁剂的是B(填字母序号);
A.铁锈 B.油污 C.水垢

(3)“污渍爆炸盐”溶于水后会生成Na2CO3和H2O2.将爆炸盐溶于水后,再加入足量的洁厕灵,产生能使澄清石灰水变浑浊的气体,此反应体现了图1中②(选填①②③④)盐的性质关系;
(4)将洁厕灵滴入炉具清洁剂中,如图2甲所示.
①若反应后溶液呈红色,则反应后溶液中的溶质是(酚酞除外)NaCl、NaOH,此时溶液可用图2乙中A(选填A、B、C)点处表示;
②若反应后溶液pH为7,图2丙中a微粒的化学式为H2O;
③丙中反应没有明显现象,为证明反应发生,可加入的试剂有ABD.
A.无色酚酞溶液 B.石灰石 C.硝酸银溶液 D.锌粒.
| A. | 偏向左边 | B. | 偏向右边 | C. | 仍指零处 | D. | 无法确定 |
| 物质 | 煤油 | 丙醇 | 四氯化碳 | 乙醚 |
| 沸点/℃ | 180-310 | 97.4 | 76.5 | 34.5 |
| A. | 煤油 | B. | 丙醇 | C. | 四氯化碳 | D. | 乙醚 |
 某化学实验小组对“影响石灰石与盐酸反应速率的因素--盐酸的浓度和石灰石的颗粒大小等”进行了如下实验探究,请你参与.
某化学实验小组对“影响石灰石与盐酸反应速率的因素--盐酸的浓度和石灰石的颗粒大小等”进行了如下实验探究,请你参与.[进行实验]
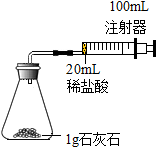
室温下,选用20mL不同溶质质量分数的盐酸(4%和6%)分别与1g颗粒状或块状的石灰石进行实验(固定夹持仪器略去).
(1)石灰石与盐酸反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)按上图装置进行实验,在装药品前应检查该装置的气密性,具体的做法是将注射器活塞向外拉出一段,松开手一会后,若活塞又回到原位,证明装置气密性良好.开始实验时,应将20mL稀盐酸快速(选填“快速”或“缓慢”)推入锥形瓶中,以保证盐酸能全部推入锥形瓶中.
[处理数据]
(3)实验小组进行实验后,获得的相关实验数据如表所示:
| 实验编号 | 盐酸溶质质量分数 (均取20mL) | 石灰石固体形状 (均取1g) | 二氧化碳体积(mL) (均收集前30S的气体) |
| a | 4% | 颗粒 | 64.0 |
| b | 4% | 块状 | 40.4 |
| c | 6% | 颗粒 | 98.2 |
| d | 6% | 块状 | 65.3 |
②从上述实验中得出石灰石的颗粒大小反应速率影响的结论是颗粒越小,反应的速率越大.
[拓展延伸]
(4)如表是实验时记录生成的二氧化碳气体体积和对应的时间的一组实验数据(每间隔4S读数一次):
| 时间/S | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | 36 | 40 |
| 气体体积/mL | 16.0 | 22.2 | 29.4 | 39.3 | 50.4 | 57.6 | 62.0 | 64.7 | 66.0 | 66.0 |
(5)你认为影响石灰石与盐酸反应速率的因素还有石灰石的纯度,请设计实验方案验证你的猜想取不同地区的石灰石,保持颗粒大小以及质量相同,加入相同的盐酸,记录生成相同的二氧化碳气体体积所需要的时间,纯度越大,速率越大.

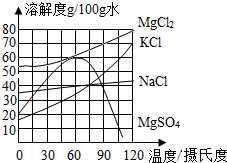 食盐在生产和生活中具有广泛的用途,是一种重要的资源,海水中储量很丰富,通过晾晒海水可以得到粗盐和卤水.如图所示为NaCl及卤水主要成分的溶解度曲线图.
食盐在生产和生活中具有广泛的用途,是一种重要的资源,海水中储量很丰富,通过晾晒海水可以得到粗盐和卤水.如图所示为NaCl及卤水主要成分的溶解度曲线图.