题目内容
1.做电解水实验时,要给水通电.正极玻璃管内得到的气体体积较小(“大”或“小”)是氧气;负极玻璃管内得到的气体体积较大(“大”或“小”),是氢气.这个反应的化学方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,此反应属于分解反应.分析 本题主要考查电解水实验的现象和结论,还涉及文字表达式的书写和反应类型的判断,解题时要依据所学知识和实验经验来解答.
解答 解:电解水实验要用直流电源,在电解水实验中,可观察到的现象有:正极的气体体积少,能使带火星的木条复燃,负极的气体体积多,能燃烧,而且体积多的是少的二倍.根据以上现象可推出正极产生的气体是氧气,负极产生的气体是氢气,发生反应的化学方程式为:2H2O $\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,该变化是由一种物质变成多种物质的反应,属于分解反应.
故答案为:小;氧;大;氢;2H2O $\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;分解.
点评 本题属于基础知识的考查,只要平时能认真读课本并积极参与实验观察,即可较轻易地回答,但试验中需要用直流电,容易被忽视,因此要重视实验中的细节问题.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
13.下列实验现象描述正确的是( )
| A. | 铁丝在氧气中燃烧:银白色固体剧烈燃烧,火星四射,放出大量的热,生成黑色固体 | |
| B. | 高温条件下木炭还原氧化铜:黑色固体逐渐变成光亮的铜 | |
| C. | 电解水实验:两个电极附近产生气泡,一段时间后,正、负极产生的气体体积比约为2:1 | |
| D. | 铜片放人硝酸银溶液中:紫红色固体表面有银白色固体产生,溶液由蓝色逐渐变为无色 |
14.金属与人类的生活和生产密切相关.
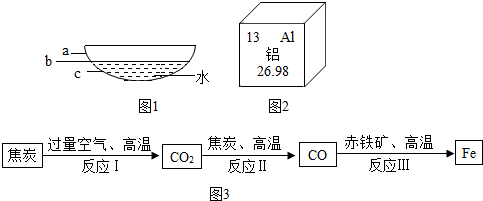
(1)图1为放置在空气中的铁锅,其中最容易生锈的部位是b(填字母代号).
(2)图2为元素周期表中的一格,下列说法不正确的是C.
A.铝是地壳中含量最多的金属元素
B.铝原子的核外电子数为l3
C.铝元素的原子结构示意图为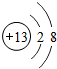
D.铝元素的相对原子质量为26.98
(3)在研究金属性质时,某小组同学进行了如下实验探究:将一定量铁粉加入到硫酸锌和硫酸铜的混合溶液中,充分反应后过滤,然后对滤纸上的物质进行分析和实验.
【提出问题】滤纸上的物质是什么?
【做出猜想】甲认为只有铜;乙认为是铜和铁的混合物;丙认为是铜、铁、锌的混合物.
【交流讨论】大家一致认为丙的猜想不合理,其理由是锌比铁活泼,铁不能置换硫酸锌中的锌.
【实验与结论】同学们通过实验确定了滤纸上物质的成分.请填写如表空白.
(4)钢铁是人类生活和生产中非常重要的材料.
①工业炼铁的反应过程如图3所示.其中焦炭的作用是为了生成还原剂一氧化碳;属于化合反应的是反应Ⅰ和反应Ⅱ.
②在工业冶炼中要得到224t铁,理论上需要含Fe2O380%的赤铁矿石的质量是多少?

(1)图1为放置在空气中的铁锅,其中最容易生锈的部位是b(填字母代号).
(2)图2为元素周期表中的一格,下列说法不正确的是C.
A.铝是地壳中含量最多的金属元素
B.铝原子的核外电子数为l3
C.铝元素的原子结构示意图为
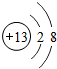
D.铝元素的相对原子质量为26.98
(3)在研究金属性质时,某小组同学进行了如下实验探究:将一定量铁粉加入到硫酸锌和硫酸铜的混合溶液中,充分反应后过滤,然后对滤纸上的物质进行分析和实验.
【提出问题】滤纸上的物质是什么?
【做出猜想】甲认为只有铜;乙认为是铜和铁的混合物;丙认为是铜、铁、锌的混合物.
【交流讨论】大家一致认为丙的猜想不合理,其理由是锌比铁活泼,铁不能置换硫酸锌中的锌.
【实验与结论】同学们通过实验确定了滤纸上物质的成分.请填写如表空白.
| 实验步骤 | 现象和结论 | 有关反应的化学方程式 |
| 取少量滤纸上剩余的物质,加入适量的溶液 | 若产生气泡,则乙猜想正确,若不产生气泡,则甲猜想正确 | Fe+2HCl═FeCl2+H2↑ |
①工业炼铁的反应过程如图3所示.其中焦炭的作用是为了生成还原剂一氧化碳;属于化合反应的是反应Ⅰ和反应Ⅱ.
②在工业冶炼中要得到224t铁,理论上需要含Fe2O380%的赤铁矿石的质量是多少?
13.下列实验操作或数据中,正确的是( )
| A. | 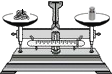 称量10.05g固体 | B. | 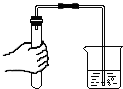 检查气密性 | C. | 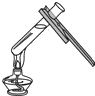 加热液体 | D. |  量取9.5mL液体 |