题目内容
15.向AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,反应完成后过滤,下列情况可能存在的是( )| A. | 滤纸上有Ag、Cu、Fe、Zn,滤液中有Zn2+、Fe2+ | |
| B. | 滤纸上有Ag,滤液中有Zn2+、Fe2+ | |
| C. | 滤纸上有Ag、Cu,滤液中有Cu2+、Zn2+、Fe2+ | |
| D. | 滤纸上有Ag、Cu、Fe,滤液中有Cu2+、Zn2+、Fe2+ |
分析 在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此分析判断.
解答 解:由于金属的活动性顺序是:Zn>Fe>Cu>Ag,向AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,铁粉首先与AgNO3溶液反应,当AgNO3溶液反应完全后再与Cu(NO3)2溶液反应,不能与Zn(NO3)2的溶液反应.
A、由于铁不能与Zn(NO3)2的溶液反应,滤纸上不可能有Zn,故A错误;
B、滤纸上有Ag没有Cu,溶液就有Cu2+,故B错误;
C、当铁的量不足,只能置换出部分铜时,滤纸上有Ag、Cu,滤液中有Cu2+、Zn2+、Fe2+,故C正确;
D、纸上有Fe时,溶液不可能有Cu2+,故D错误.
故选C.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
5.煤炉火焰越扇越旺,而蜡烛火焰一扇就灭,以下对该现象的分析正确的是( )
| A. | 扇蜡烛会隔绝空气 | B. | 扇蜡烛会石蜡着火点 | ||
| C. | 扇煤炉会增大空气进入量 | D. | 扇煤炉会增加新的易燃物 |
6. 在一定条件下发生的某个化学反应如图所示,下列说法总正确的是( )
在一定条件下发生的某个化学反应如图所示,下列说法总正确的是( )
 在一定条件下发生的某个化学反应如图所示,下列说法总正确的是( )
在一定条件下发生的某个化学反应如图所示,下列说法总正确的是( )| A. | 反应是化合反应 | B. | 反应物都是化合物 | ||
| C. | 反应前后微粒种类未发生变化 | D. | 反应可能是:H2O+Cl2═HClO+HCl |
20.下列物质属于氧化物的是( )
| A. | 氧气 | B. | 四氧化三铁 | C. | 碳酸钠 | D. | 氢氧化钙 |
4.下列中学生营养餐的食品中,含丰富蛋白质的是( )
| A. | 馒头 | B. | 大米粥 | C. | 鸡蛋 | D. | 炒青菜 |
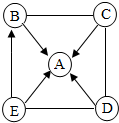 A-E是初中化学常见的化合物,它们相互关系如图所示,图中“→”表示转化关系.“--”表示相互能反应(部分物质和反应条件未标出).已知B是常用于灭火的气体,且与A、E属于同类物质.
A-E是初中化学常见的化合物,它们相互关系如图所示,图中“→”表示转化关系.“--”表示相互能反应(部分物质和反应条件未标出).已知B是常用于灭火的气体,且与A、E属于同类物质.