题目内容
根据所示实验示意图回答问题:
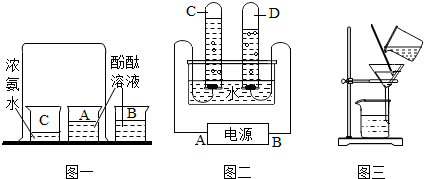
(1)图一实验中, (填序号)烧杯中溶液变红,该实验不能证明 (填序号).
①分子小 ②分子在不断运动 ③构成物质的分子不同,性质不同 ④分子由原子构成
(2)图二水的电解实验中,该实验得出的结论是 (填序号).
①水由氢氧元素组成 ②水由氢气和氧气组成 ③水由水元素组成
水电解时,加入少量的氢氧化钠可以增强水的导电性,现将0.1g氢氧化钠溶解在99.9g水里,接通电源,当正极产生气体的质量为32g时,剩下溶液中氢氧化钠的质量分数为 (准确到0.01%).
(3)图三所示过滤操作中,玻璃棒的作用是 ,过滤时速率慢的作用是 (填序号).
①滤纸破损 ②滤纸未紧贴漏斗内壁 ③固体堵塞滤纸 ④液面高于滤纸边缘.

(1)图一实验中,
①分子小 ②分子在不断运动 ③构成物质的分子不同,性质不同 ④分子由原子构成
(2)图二水的电解实验中,该实验得出的结论是
①水由氢氧元素组成 ②水由氢气和氧气组成 ③水由水元素组成
水电解时,加入少量的氢氧化钠可以增强水的导电性,现将0.1g氢氧化钠溶解在99.9g水里,接通电源,当正极产生气体的质量为32g时,剩下溶液中氢氧化钠的质量分数为
(3)图三所示过滤操作中,玻璃棒的作用是
①滤纸破损 ②滤纸未紧贴漏斗内壁 ③固体堵塞滤纸 ④液面高于滤纸边缘.
考点:分子的定义与分子的特性,过滤的原理、方法及其应用,电解水实验
专题:实验性简答题
分析:(1)根据浓氨水具有挥发性,会挥发出氨气,氨气溶于水显碱性,能使酚酞试液变红进行解答;
(2)根据水通电分解生成氢气和氧气以及正极生成氧气进行解答;
(3)根据过滤时玻璃棒的作用是引流以及过滤的注意事项进行解答.
(2)根据水通电分解生成氢气和氧气以及正极生成氧气进行解答;
(3)根据过滤时玻璃棒的作用是引流以及过滤的注意事项进行解答.
解答:解:(1)浓氨水具有挥发性,会挥发出氨气,氨气溶于水显碱性,能使酚酞试液变红,所以图一实验中,A烧杯中溶液变红,该实验证明分子在不断运动、构成物质的分子不同,性质不同,但是不能证明分子很小、分子由原子构成;故填:A;①④;
(2)水通电分解生成氢气和氧气,所以可知水由氢氧元素组成,正极生成氧气,正极产生气体的质量为32g,即氧气的质量为32,
设消耗水的质量为x
2H2O
2H2↑+O2↑
36 32
x 32g
=
x=36g
剩下溶液中氢氧化钠的质量分数为=
×100%=0.16%
答:剩下溶液中氢氧化钠的质量分数为0.16%;
故答案为:①;0.16%;
(3)过滤时玻璃棒的作用是引流;过滤时速率慢的作用是滤纸未紧贴漏斗内壁、固体堵塞滤纸.故填:引流;②③.
(2)水通电分解生成氢气和氧气,所以可知水由氢氧元素组成,正极生成氧气,正极产生气体的质量为32g,即氧气的质量为32,
设消耗水的质量为x
2H2O
| ||
36 32
x 32g
| 36 |
| x |
| 32 |
| 32g |
x=36g
剩下溶液中氢氧化钠的质量分数为=
| 0.1g |
| 0.1g+99.9g-36g |
答:剩下溶液中氢氧化钠的质量分数为0.16%;
故答案为:①;0.16%;
(3)过滤时玻璃棒的作用是引流;过滤时速率慢的作用是滤纸未紧贴漏斗内壁、固体堵塞滤纸.故填:引流;②③.
点评:本题主要考查酸碱指示剂的变色规律及其性质、水通电分解实验以及过滤的注意事项;学会分析反应现象和本质的联系;并会利用分子与原子的性质分析和解决问题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
通常的食醋中约含3%~5%的乙酸(化学式为C2H4O2).有关乙酸的说法,正确的是( )
| A、乙酸含有2个碳元素、4个氢元素、2个氧元素 |
| B、乙酸由碳原子、氢原子、氧原子构成 |
| C、乙酸是一种化合物 |
| D、乙酸分子中含有氧分子 |
今年9月27日,日本御岳山火山喷发,造成多人伤亡.火山灰里含有大量的硅酸钙(CaSiO3),硅酸钙中硅元素的化合价为( )
| A、+3 | B、+4 | C、+5 | D、-4 |
诗词是民族灿烂文化的瑰宝.下列著名诗句中只含有物理变化的是( )
| A、野火烧不尽,春风吹又生 |
| B、爆竹声中一岁除,春风送暖入屠苏 |
| C、夜来风雨声,花落知多少 |
| D、春蚕到死丝方尽,蜡炬成灰泪始干 |
 元素周期表是学习化学的重要工具,如图是元素周期表的一个小格,从中获得信息正确的是( )
元素周期表是学习化学的重要工具,如图是元素周期表的一个小格,从中获得信息正确的是( )| A、该元素核内有20个质子 |
| B、该元素为非金属元素 |
| C、该元素的相对质子质量为40.08g |
| D、该元素的中子数为40.8 |
有一瓶无色气体,可能是二氧化碳气体,你认为应该用下述哪种方法确定( )
| A、实验 | B、调查 |
| C、上网查询 | D、讨论 |
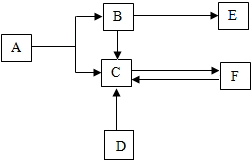 A-F是初中常见的物质,有如图所示的转化关系,其中A、B为无色液体,C、E、F
A-F是初中常见的物质,有如图所示的转化关系,其中A、B为无色液体,C、E、F