题目内容
14.在实验室用加热高锰酸钾的方法制取氧气,请你计算用3.16g高锰酸钾理论上可制得氧气的质量是多少?分析 利用高锰酸钾受热分解的化学方程式,根据高锰酸钾的质量求出氧气的质量.
解答 解:设可制得氧气的质量为x
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
3.16g x
$\frac{316}{3.16g}=\frac{32}{x}$
解得:x=0.32g
答:用3.16g高锰酸钾理论上可制得氧气的质量是0.32克.
点评 利用化学方程式计算,首先必须读懂题意,然后根据化学方程式的计算步骤进行.注意的要点有:正确地写出反应的化学方程式、准确的计算出相关物质的相对分子质量、化学方程式中任意两种物质之间都存在固定的比例关系,解题的过程要规范.

练习册系列答案
相关题目
20.在一定温度下,有一杯完全溶解的、饱和的氯化铵溶液,如果想把它变为不饱和溶液,下列可采 取的指施有(已知氯化铵固体的溶解度随温度的升高而增大)①降低温度②升高温度③加氯化铵固体④加溶剂⑤恒温蒸发溶剂( )
| A. | ①③④ | B. | ①③⑤ | C. | ②④ | D. | ②⑤ |
5.在密闭容器内有M.N.O.P四种物质,一定条件下发生反应,一段时间后.则得反应前后各物质的质量关系如下表所示
下列有关此反应的说法中错误的是( )
| 物质 | M | N | O | P |
| 反应前质量/g | 18 | 1 | 2 | 32 |
| 反应后质量/g | X | 26 | 2 | 12 |
| A. | 反应后X的质量为13g | B. | 该反应为化合反应 | ||
| C. | 参加反应的M、P的质量比为9:16 | D. | O物质可能是催化剂 |
2.下列实验或者操作方法能达到目的是( )
| 选项 | 要求 | 操作方法 |
| A | 检测溶液的酸碱度 | 加入酸碱指示剂,观察颜色变化 |
| B | 检测溶液是否为碱溶液 | 测定溶液的PH值 |
| C | 除去火碱溶液中的少量纯碱 | 加入适量氯化钡溶液,反应后过滤 |
| D | 除去水中的双氧水 | 适当加热或加入少量MnO2充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
9.下列物质中,属于有机物的是( )
| A. | 氢氧化钙[Ca(OH)2] | B. | 氯化钠[NaCl] | C. | 硫酸[H2SO4] | D. | 甲烷[CH4] |
19.煤是使用广泛的化石燃料,但直接燃烧会导致空气污染,产生的气体中会形成酸雨的是( )
| A. | CO2 | B. | SO2 | C. | CO | D. | H2O |
6.在元素周期表中,硫元素的信息如图所示,下列从图中获得的信息不正确的是( )

| A. | 由硫的原子结构示意图可以得出a+b+6=X | |
| B. | 硫原子在化学反应中易获得2个电子形成S2- | |
| C. | 该元素为非金属元素 | |
| D. | 硫原子的相对原子质量是32.06g |
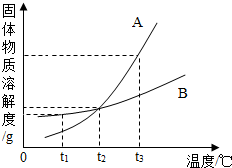 如图是A、B两种物质的溶解度曲线,根据图示回答下列问题:
如图是A、B两种物质的溶解度曲线,根据图示回答下列问题: