题目内容
6.木炭还原氧化铜实验后的混合粉末中含有铜、氧化铜、木炭粉,某化学实验小组设计回收铜的方案如下: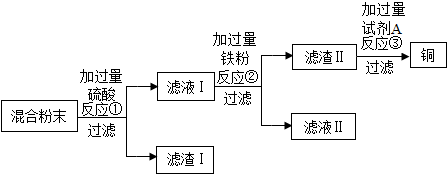
(1)过滤操作中必须用到的玻璃仪器有烧杯、漏斗和玻璃棒.
(2)反应①的化学方程式为H2SO4+CuO═CuSO4+H2O.
(3)滤液Ⅱ中的溶质为硫酸亚铁.
(4)试剂A最好选用下列②溶液(填序号).
①H2SO4 ②CuSO4 ③MgSO4
(5)为了完善实验方案,可对滤渣Ⅰ中的Cu进行回收.
分析 (1)根据过滤时所用仪器解答;
(2)根据反应流程及反应物和生成物写出化学方程式;
(3)根据反应流程分析解答;
(4)要除去铜粉中的铁粉,可加入硫酸铜;
(5)要得到更多的铜,可将反应过程中的铜全部回收
解答 解:
(1)根据过滤时所用仪器可知,必须用到的玻璃仪器有烧杯、玻璃棒和漏斗;
(2)氧化铜与硫酸反应生成硫酸铜和水,铜、木炭与硫酸不反应,化学方程式为:H2SO4+CuO═CuSO4+H2O;
(3)反应①后,滤液1中的溶质是硫酸和硫酸铜,过滤后的滤液中加入过量铁粉,硫酸铜和铁粉反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4═FeSO4+Cu,H2SO4+Fe═FeSO4+H2↑;滤液Ⅱ中的溶质为硫酸亚铁;
(4)滤渣Ⅱ中含有剩余的铁粉,经过③后得到铜,可知除去过量的铁粉,最好用硫酸铜溶液;
(5)开始混合粉末中的铜没有和酸反应,进入滤渣Ⅰ中,为了回收更多的铜,可将滤渣Ⅰ中的铜也回收.
答案:
(1)玻璃棒;
(2)H2SO4+CuO═CuSO4+H2O;
(3)硫酸亚铁;
(4)②;
(5)Cu.
点评 对于流程图的题目关健是看明白流程图中各物质的转化关系,注意过量物质的去向,如何除去过量物质.

练习册系列答案
相关题目
16.在地震灾害后的防疫工作中,人们用二氧化氯(C1O2)作消毒剂.C1O2是-种橙绿色、有刺激性气味的气体,11℃以下为红色液体,易溶于水,见光易分解.下列描述属于二氧化氯化学性质的是( )
| A. | 橙绿色 | B. | 有刺激性气味 | C. | 见光易分解 | D. | 易溶于水 |
1.下列去除杂质方法中正确的是( )
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | CaCl2溶液 | 稀盐酸 | 加过量碳酸钙,过滤 |
| B | K2CO3溶液 | KCl | 加适量稀盐酸 |
| C | CaO | CaCO3 | 加水,过滤 |
| D | NaCl溶液 | Na2CO3 | 加适量硝酸钙溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
11.化学是一门以实验为基础的科学,许多化学重大发现和研究成果都是通过实验得到的.下列实验操作或设计中正确的是( )
| A. | 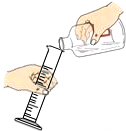 用100mL量筒量取8.5mL盐酸 | B. | 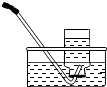 收集氧气 | ||
| C. | 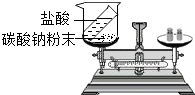 验证质量守恒定律 | D. | 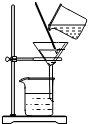 分离碘酒中的碘 |
18.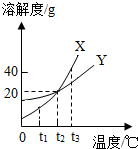 如图是X、Y两种固体物质的溶解度曲线.下列说法中正确的是( )
如图是X、Y两种固体物质的溶解度曲线.下列说法中正确的是( )
 如图是X、Y两种固体物质的溶解度曲线.下列说法中正确的是( )
如图是X、Y两种固体物质的溶解度曲线.下列说法中正确的是( )| A. | X的溶解度大于Y的溶解度 | |
| B. | t2℃时X的饱和溶液比Y的不饱和溶液质量分数大 | |
| C. | t1℃时X和Y的饱和溶液升温到t2℃时两者溶质的质量分数相等 | |
| D. | t3℃时X和Y的饱和溶液降温到t1℃时析出晶体较多的是X |
15.下列物质的用途不正确的是( )
| A. | NaCl常用作调味品 | B. | NaHCO3用于治疗胃酸过多 | ||
| C. | BaCO3用作钡餐透视 | D. | Na2CO3用于生产洗涤剂 |