题目内容
10.用化学用语填:(1)3个氢离子3H+.
(2)碘酒中的溶剂C2H5OH.
(3)人体中含量最多的金属元素Ca.
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:(1)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字,故3个氢离子可表示为:3H+.
(2)碘酒是碘的酒精溶液,碘酒中的溶剂是酒精,其化学式为:C2H5OH.
(3)根据人体中含量最多的金属元素是钙,元素符号为:Ca;
故答案为:(1)3H+;(2)C2H5OH;(3)Ca;
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
7. 中和反应是一类重要的反应.根据要求回答问题:
中和反应是一类重要的反应.根据要求回答问题:
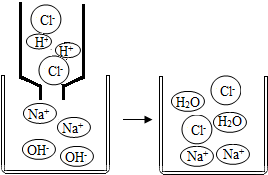
(1)许多物质在溶液中以离子形式存在.如图表示HCl、NaOH溶液及两者混合后溶质在溶液中的存在情况.
①盐酸具有酸的特性,是因为盐酸溶液中含有H+(填微粒符号).
②对比分析盐酸与氢氧化钠溶液混合前后溶液离子存在情况,可知两者反应时不会减少的离子是Cl-、Na+.
③教材指出:酸与碱中和反应的结果是酸和碱各自的特性都消失.请结合图并从微粒的角度分析,盐酸与氢氧化钠反应时,为何酸、碱各自的特性都消失?答:氢离子和氢氧根离子结合生成了水.
(2)日常生活中,凡是使酸的酸性消失或碱的碱性消失的反应均被称为“中和”.如使用碳酸氢钠(其溶液显碱性)治疗胃酸(主要成分为盐酸)过多症,就因碳酸氢钠能使胃酸的酸性消失,而称为碳酸氢钠“中和”了过多的胃酸.现有碳酸氢钠溶液、酚酞溶液和盐酸溶液,设计实验证明碳酸氢钠溶液与盐酸反应时,碳酸氢钠溶液的碱性、盐酸的酸性都将各自消失.
 中和反应是一类重要的反应.根据要求回答问题:
中和反应是一类重要的反应.根据要求回答问题:(1)许多物质在溶液中以离子形式存在.如图表示HCl、NaOH溶液及两者混合后溶质在溶液中的存在情况.
①盐酸具有酸的特性,是因为盐酸溶液中含有H+(填微粒符号).
②对比分析盐酸与氢氧化钠溶液混合前后溶液离子存在情况,可知两者反应时不会减少的离子是Cl-、Na+.
③教材指出:酸与碱中和反应的结果是酸和碱各自的特性都消失.请结合图并从微粒的角度分析,盐酸与氢氧化钠反应时,为何酸、碱各自的特性都消失?答:氢离子和氢氧根离子结合生成了水.
(2)日常生活中,凡是使酸的酸性消失或碱的碱性消失的反应均被称为“中和”.如使用碳酸氢钠(其溶液显碱性)治疗胃酸(主要成分为盐酸)过多症,就因碳酸氢钠能使胃酸的酸性消失,而称为碳酸氢钠“中和”了过多的胃酸.现有碳酸氢钠溶液、酚酞溶液和盐酸溶液,设计实验证明碳酸氢钠溶液与盐酸反应时,碳酸氢钠溶液的碱性、盐酸的酸性都将各自消失.
| 操作 | 现象 | 结论 |
| 实验1:往装有碳酸氢钠溶液的试管中先加入2-3滴酚酞溶液,再逐滴加入盐酸直至恰好完全反应 | 滴入酚酞时的现象:酚酞变成红色; 逐滴加入盐酸的现象:有气泡冒出,且溶液逐渐变成无色. | 两者反应时,碳酸氢钠溶液碱性消失 |
| 实验2:往装有盐酸的试管中先加入2-3滴酚酞溶液,再逐滴加入足量的碳酸氢钠溶液 | 酚酞不变色;加入碳酸氢钠,溶液中出现气泡,无色酚酞变成红色. | 两者反应时,盐酸溶液酸性消失 |
1.水蒸气通过红热的铁粉,发生的反应为:3Fe+4H2O═X+4H2,则X为( )
| A. | FeO | B. | Fe2O3 | C. | Fe3O4 | D. | Fe(OH)2 |
18.某化学兴趣小组的同学在整理实验室时发现一瓶氢氧化钠固体,于是他们对这瓶氨氧化钠固体的成分展开探究.
【提出问题】这瓶氢氧化钠固体是否变质?若发生变质,则变质的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示)
【猜想假设】猜想一:没有变质;’
猜想二:完全变质
猜想三:部分变质;
【实验探究】为了探究固体成分,他们分别进行了如下实验:
(1)甲同学取少量固体于试管中,加入稀硫酸,产生了较多气泡,他认为这瓶固体中含有Na2CO3,从而否定了猜想一.
(2)为了进一步确定这包固体的成分,乙同学取少量固体于试管中,加水溶解后滴入酚酞溶液变红,于是他认为猜想三正确.
(3)丙同学认为乙的结论不严密,于是设计了以下方案,请你完成下列实验报告:
【反思与交流】
(4)要除去久置的氢氧化钠固体中的杂质,得到纯净的氢氧化钠,可用Ca(OH)2+Na2CO3═CaCO3↓+2NaOH(用化学方程式表示)•
【提出问题】这瓶氢氧化钠固体是否变质?若发生变质,则变质的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示)
【猜想假设】猜想一:没有变质;’
猜想二:完全变质
猜想三:部分变质;
【实验探究】为了探究固体成分,他们分别进行了如下实验:
(1)甲同学取少量固体于试管中,加入稀硫酸,产生了较多气泡,他认为这瓶固体中含有Na2CO3,从而否定了猜想一.
(2)为了进一步确定这包固体的成分,乙同学取少量固体于试管中,加水溶解后滴入酚酞溶液变红,于是他认为猜想三正确.
(3)丙同学认为乙的结论不严密,于是设计了以下方案,请你完成下列实验报告:
| 实验步骤 | 可能观察到的现象 | 结论 |
| ①取样于试管中,加水溶解,滴入过量的 BaCl2 (填化学式)溶液 | 产生白色沉淀 | 猜想二正确 |
| ②反应后过滤,取上层清液,滴入酚酞溶液 | 溶液不变色 |
(4)要除去久置的氢氧化钠固体中的杂质,得到纯净的氢氧化钠,可用Ca(OH)2+Na2CO3═CaCO3↓+2NaOH(用化学方程式表示)•
5.下列物质的化学式与俗称、用途相符合的是( )
| A. | Na2CO3 小苏打 用于造纸行业 | B. | Ca(OH)2 消石灰 处理酸性废水 | ||
| C. | CaCO3 生石灰 补钙剂 | D. | NaOH 纯碱 除油污 |