题目内容
14.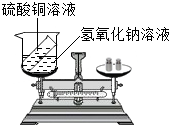 某兴趣小组为了验证质量守恒定律,在烧杯中盛有20g溶质质量分数为20%的氢氧化钠溶液试管内装有20g硫酸铜溶液,如图所示,放于天平上称量,此时天平平衡.然后将试管内药品倒入烧杯内(试管不取出),恰好完全反应,试根据要求,回答下列问题:
某兴趣小组为了验证质量守恒定律,在烧杯中盛有20g溶质质量分数为20%的氢氧化钠溶液试管内装有20g硫酸铜溶液,如图所示,放于天平上称量,此时天平平衡.然后将试管内药品倒入烧杯内(试管不取出),恰好完全反应,试根据要求,回答下列问题:(1)写出实验过程中观察到的一项实验现象:出现蓝色沉淀.
(2)反应结束后,天平指针会不发生偏转 (填“偏左”“偏右”“不发生偏转”之一).
(3)试计算恰好完全反应时所得不饱和溶液的质量.(精确到0.1g)
分析 氢氧化钠和硫酸铜反应生成蓝色沉淀氢氧化铜和硫酸钠;
化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和.
解答 解:(1)实验过程中观察到:产生蓝色沉淀,天平仍然平衡.
故填:出现蓝色沉淀.
(2)因为反应不产生气体,因此反应结束后,天平指针不发生偏转.
故填:不发生偏转.
(3)设生成氢氧化铜的质量为x,
2NaOH+CuSO4═Na2SO4+Cu(OH)2↓,
80 98
20g×20% x
$\frac{80}{20g×20%}$=$\frac{98}{x}$,
x=4.9g,
恰好完全反应时所得不饱和溶液的质量为:20g+20g-4.9g=35.1g,
答:恰好完全反应时所得不饱和溶液的质量是35.1g.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
5.下列有关物质用途的说法正确的是( )
| A. | 碳酸钡是医院常用的钡餐 | B. | 利用活性炭的吸附性可将硬水软化 | ||
| C. | 氢氧化钠溶液可以干燥某些气体 | D. | 氢氧化镁可用于治疗胃酸过多 |
19.下列属于同一物质的一组是( )
| A. | 冰和干冰 | B. | 石墨和金刚石 | C. | 熟石灰和石灰石 | D. | 苏打和纯碱 |
6.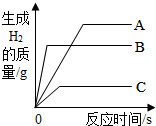 将形状相同、质量相等的A、B、C三种金属,分别放入三份溶质质量分数相同且足量的稀盐酸中,生成H2的质量与反应时间关系如图所示.已知:A、B、C在生成物中均为+2价,根据图中信息,结论正确的是( )
将形状相同、质量相等的A、B、C三种金属,分别放入三份溶质质量分数相同且足量的稀盐酸中,生成H2的质量与反应时间关系如图所示.已知:A、B、C在生成物中均为+2价,根据图中信息,结论正确的是( )
 将形状相同、质量相等的A、B、C三种金属,分别放入三份溶质质量分数相同且足量的稀盐酸中,生成H2的质量与反应时间关系如图所示.已知:A、B、C在生成物中均为+2价,根据图中信息,结论正确的是( )
将形状相同、质量相等的A、B、C三种金属,分别放入三份溶质质量分数相同且足量的稀盐酸中,生成H2的质量与反应时间关系如图所示.已知:A、B、C在生成物中均为+2价,根据图中信息,结论正确的是( )| A. | 金属活动性:A>B>C | B. | 放出H2的质量:A>B>C | ||
| C. | 相对原质量:C>A>B | D. | 若B为镁,则A可能是铁 |
4.甲醛是一种有毒物质,可用作农药和消毒剂,下列关于甲醛(CH2O)的说法错误的是( )
| A. | 从类别上看:甲醛属于有机物 | |
| B. | 从变化上看:甲醛完全燃烧生成水和二氧化碳 | |
| C. | 从宏观上看:甲醛由碳、氢、氧三种元素组成 | |
| D. | 从微观上看:甲醛由1个碳原子、2个氢原子和1个氧原子构成 |