题目内容
20℃时,10 g食盐能溶解在100 g水中,所以食盐在20℃时的溶解度是10 g,这种说法是否正确?
解析:
|
解答:错误.因为20℃时,10 g食盐溶于100 g水中形成的是不饱和溶液,所以20℃时氯化钠溶解度不是10 g. 分析:固体物质在水中溶解的量与下列因素有关: (1)温度 大多数饱和溶液升温后会变成不饱和溶液. (2)一定量的溶剂 溶剂量增加,可溶解的溶质质量增大. 所以溶解度要强调一定的温度、100 g溶剂、饱和溶液三个条件. |

 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案(一)原料岩盐水主要含氯化钠,此外还含有较多硫酸钠,以及少量氯化钙和氯化镁.上述几种物质在不同温度时的溶解度数据如下表:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 硫酸钠 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| 氯化镁 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 | |
(2)10℃时由100g水配制得到的饱和硫酸钠溶液中溶质的质量是
(二)岩盐水初步处理后,经净化、精制得到生产碳酸钠所需要的食盐水,同时制取副产品A晶体,其主要流程如下:
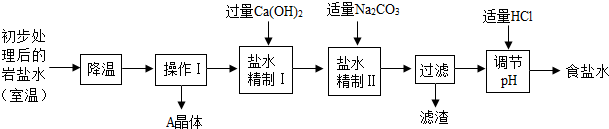
(3)“降温”的目的是析出副产品“A晶体”,A的化学式是
(4)“操作I”中的操作是
(5)“盐水精制I”是除去盐水中的少量氯化镁,反应的化学方程式是
(6)“盐水精制Ⅱ”是除去盐水中的其他杂质,反应的化学方程式是
下表是KNO3、NaCl在不同温度下的溶解度。
|
温度(℃) |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
100 |
|
KNO3 |
13.3 |
20.9 |
32 |
45.8 |
64 |
85.5 |
110 |
138 |
169 |
202 |
245 |
|
NaCl |
35.7 |
35.8 |
36 |
36.3 |
36.6 |
37 |
37.3 |
37.8 |
38.4 |
39 |
39.8 |
(1)依据上表数据,绘制KNO3、NaCl的溶解度曲线,下图1中能表示KNO3溶解度曲线的是_________________。(填“a”或“b”)
(2)下图1中P点的含义是__________________________________。

(3)欲使硝酸钾不饱和溶液转化为饱和溶液,可以采取的方法之一是_______________。
(4)30℃时,在两个各盛有100g水的烧杯中,分别加入相同质量的氯化钠和硝酸钾,充分溶解后,其结果如上图2所示,加入的甲物质是_________________。

(5)硝酸钾中含有少量氯化钠时,可通过_________________(填“蒸发结晶”或“降温结晶”)的方法提纯。
(6)20℃时,136g饱和食盐水,蒸发10g水后,再降温到20℃,可析出NaCl晶体的质量为________g。
(7)60℃时,将60g硝酸钾放入盛有50g水的烧杯中,充分搅拌,所得溶液的质量为________g。
追踪科学家的足迹
材料1:纯碱的产量是衡量一个国家化学工业发展水平的重要指标。下面是实验室摸拟侯氏制碱法生产原理的主要过程:
(1)20℃时,向浓氨水中通入足量的二氧化碳得到NH4HCO3饱和溶液;
②向NH4HCO3饱和溶液中加入食盐细粒,并不断搅拌,直到NaHCO3结晶析出完毕;
③将析出的晶体过滤,得到晶体和滤液,洗涤晶体,然后将晶体放在试管中充分加热,得到Na2CO3;
④向③的滤液中加入食盐细粒,析出NH4CI晶体,过滤,得到NH4CI。
材料2:四种盐在不同温度下的溶解度表。
|
盐 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NH4HCO3 | 15.8 | 21.0 | 27.0 | ------ | ------ |
| NaHCO3 | 8.1 | 9.6 | 11.1 | 12.7 | ---- |
| NH4CI | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
试回答下列问题:
(1)在实验室中,你选择的制备C02反应的化学方程式为 。在工业生产中,要获得生产纯碱的原料CO2 你认为最经济实用的方法是以 为原料,该反应的化学方程式为 。
(2)有人认为侯氏制碱法有以下优点,你认为其中正确的是 。
A.生产过程中部分反应产物可作为原料循环使用
B.副产品是一种氮肥
C.反应都不需要加热,可节约能源
(3)检验③中的白色粉末中是否含有氯化钠的方法是 。
(4)在②中,随着食盐的逐渐加入,溶液变成了NH4HCO3和NaCl的混合溶液,析出晶体之前,混合溶液中存在的离子有(用离子符号表示,下同。) 。在③中,将析出的晶体过滤后,溶液中数量减少的离子有 ;滤液中仍然存在的离子有 。②中反应的化学方程式为 。
(5)在20 ℃时,向含NH4HC03 21 g的饱和溶液中加入足量食盆。试通过计算说明,随着食盐的逐渐加入,为什么会有NaHC03晶体析出,而没有NH4CI晶休析出?理论上能析出多少克NaHCO3?(友情提示:本小题没有计算过程不得分.可能用到的相对分子质量:NH4HC03: 79; NaCl: 58.5; NaHC03: 84-, NH4CI: 53.5)。


 温度
温度