题目内容
由干燥的氯酸钾和二氧化锰组成的固体混合物的质量为8克,把该固体混合物放入大试管中加热,反应完全后,冷却到反应前的温度,称得试管中固体物质的质量为5.6克.(1)此反应的化学方程式为
(2)制得氧气的质量是
(3)原固体混合物中二氧化锰的质量是
分析:根据化学方程式计算的步骤有:一设、二写、三找、四列、五答、六查.在本题中,反应前后固体出现了差值,根据质量守恒定律,减少的质量是氧气的质量.根据氧气的质量求氯化钾的质量,固体残渣是氯化钾和二氧化锰的混合物,因此用5.6克减去氯化钾的质量就等于二氧化锰的质量.
解答:解:由题意知,生成氧气的质量为8g-5.6g=2.4g
设反应中生成KCl的质量为x.
2KClO3
2KCl+3O2↑
149 96
x 2.4g
=
x=3.725g
MnO2的质量为:5.6g-3.725g=1.875g
故答案为:
(1)2KClO3
2KCl+3O2↑;
(2)2.4g;
(3)1.875g.
设反应中生成KCl的质量为x.
2KClO3
| ||
| △ |
149 96
x 2.4g
| 149 |
| x |
| 96 |
| 2.4g |
x=3.725g
MnO2的质量为:5.6g-3.725g=1.875g
故答案为:
(1)2KClO3
| ||
| △ |
(2)2.4g;
(3)1.875g.
点评:本考点考查了根据化学方程式的计算,是中考计算题中经常出现的题型.做题时要注意:化学方程式要配平,始终不要忘记质量守恒定律,还要记牢“遇到差值要想气体”.本考点主要出现在填空题和计算题中.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
(12分)(1)小云从电视新闻中了解到:国家新版《生活饮用水卫生标准》已从今年7月1日起强制实施,其中饮用水消毒剂除了目前采用的液氯以外,补充了——氯胺(NH2Cl)、臭氧(O3)。
①O3中氧元素的化合价是 。
②NH2Cl由 (填数字)种元素组成,其中氮元素与氢元素的质量比是 。
③NH2Cl用消毒时,发生反应NH2Cl+X==NH3+HClO,其中X的化学式是 。
(2)小雨阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是他对氧化铜产生了探究兴趣。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| Ⅰ | 1.2g | | |
| Ⅱ | 1.2g | CuO 0.5g | |
| Ⅲ | 1.2g | MnO2 0.5g | |
②若实验Ⅱ比实验Ⅰ的“待测数据”更 (填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率。
③将实验Ⅱ反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到0.5g黑色粉末,再将黑色粉末放入试管中, 。(简述操作和现象)
【预期结论】氧化铜还能作氯酸钾的催化剂。
【评价设计】你认为小雨设计实验Ⅲ和实验Ⅱ对比的目的是 。
(3)小雪用如下图所示装置制取氧气的相关数据如下表。回答有关问题:
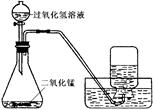
| | 气体发生装置内物质的总质量 |
| 反应前 | 35.6g |
| 反应后 | 34.8g |
②计算参加反应的过氧化氢的质量,写出必要的计算过程。
(1)小云从电视新闻中了解到:国家新版《生活饮用水卫生标准》已从今年7月1日起强制实施,其中饮用水消毒剂除了目前采用的液氯以外,补充了--氯胺(NH2Cl)、臭氧(O3).
①O3中氧元素的化合价是______.
②NH2Cl由______(填数字)种元素组成,其中氮元素与氢元素的质量比是______.
③NH2Cl用消毒时,发生反应NH2Cl+X═NH3+HClO,其中X的化学式是______.
(2)小雨阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是他对氧化铜产生了探究兴趣.
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略).
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| Ⅰ | 1.2g | ||
| Ⅱ | 1.2g | CuO 0.5g | |
| Ⅲ | 1.2g | MnO2 0.5g |
②若实验Ⅱ比实验Ⅰ的“待测数据”更______ (填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率.
③将实验Ⅱ反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到0.5g黑色粉末,再将黑色粉末放入试管中,______.(简述操作和现象)
【预期结论】氧化铜还能作氯酸钾的催化剂.
【评价设计】你认为小雨设计实验Ⅲ和实验Ⅱ对比的目的是______.
(3)小雪用如图所示装置制取氧气的相关数据如下表.回答有关问题:
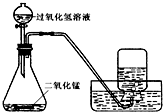 | 气体发生装置内物质的总质量 | |
| 反应前 | 35.6g | |
| 反应后 | 34.8g |
②计算参加反应的过氧化氢的质量,写出必要的计算过程.
(1)小云从电视新闻中了解到:国家新版《生活饮用水卫生标准》已从今年7月1日起强制实施,其中饮用水消毒剂除了目前采用的液氯以外,补充了--氯胺(NH2Cl)、臭氧(O3).
①O3中氧元素的化合价是______.
②NH2Cl由______(填数字)种元素组成,其中氮元素与氢元素的质量比是______.
③NH2Cl用消毒时,发生反应NH2Cl+X═NH3+HClO,其中X的化学式是______.
(2)小雨阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是他对氧化铜产生了探究兴趣.
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略).
①上述实验应测量的“待测数据”是______.
②若实验Ⅱ比实验Ⅰ的“待测数据”更______ (填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率.
③将实验Ⅱ反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到0.5g黑色粉末,再将黑色粉末放入试管中,______.(简述操作和现象)
【预期结论】氧化铜还能作氯酸钾的催化剂.
【评价设计】你认为小雨设计实验Ⅲ和实验Ⅱ对比的目的是______.
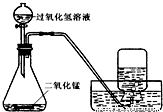
(3)小雪用如图所示装置制取氧气的相关数据如下表.回答有关问题:
①反应生成氧气的质量为______g(结果精确到0.1g,下同).
②计算参加反应的过氧化氢的质量,写出必要的计算过程.
①O3中氧元素的化合价是______.
②NH2Cl由______(填数字)种元素组成,其中氮元素与氢元素的质量比是______.
③NH2Cl用消毒时,发生反应NH2Cl+X═NH3+HClO,其中X的化学式是______.
(2)小雨阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是他对氧化铜产生了探究兴趣.
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略).
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| Ⅰ | 1.2g | ||
| Ⅱ | 1.2g | CuO 0.5g | |
| Ⅲ | 1.2g | MnO2 0.5g |
②若实验Ⅱ比实验Ⅰ的“待测数据”更______ (填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率.
③将实验Ⅱ反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到0.5g黑色粉末,再将黑色粉末放入试管中,______.(简述操作和现象)
【预期结论】氧化铜还能作氯酸钾的催化剂.
【评价设计】你认为小雨设计实验Ⅲ和实验Ⅱ对比的目的是______.
(3)小雪用如图所示装置制取氧气的相关数据如下表.回答有关问题:
| 气体发生装置内物质的总质量 | ||
| 反应前 | 35.6g | |
| 反应后 | 34.8g |
②计算参加反应的过氧化氢的质量,写出必要的计算过程.

