题目内容
5. 某校化学兴趣小组的同学在一次聚餐中,发现并对燃料固体酒精产生了好奇,于是对其成分进行了探究.
某校化学兴趣小组的同学在一次聚餐中,发现并对燃料固体酒精产生了好奇,于是对其成分进行了探究.[查阅资料](1)固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成的;
(2)氯化钙和氯化钡溶液均呈中性.
[提出问题](1)酒精中含有哪些元素?
(2)固体酒精样品中的氢氧化钠是否变质?
[实验探究]
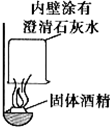
(1)按如图实验,若观察到烧杯内壁有白色固体生成,便可得出酒精燃烧产物中含有二氧化碳,只要将所用烧杯更换为冷而干燥的烧杯,即可证明燃烧产物中有水蒸汽.由上述实验现象可以推理得出酒精中所含元素的情况为含有碳元素和氢元素.
(2)他们向服务生要来少量固体酒精,放入烧杯中加并足量蒸馏水充分溶解后静置,发现烧杯底部有白色沉淀产生.取适量该白色沉淀于试管中,并向试管中滴加稀盐酸,可见沉淀溶解有气泡冒出.试用化学方程式表示出该白色沉淀的产生途径:2NaOH+CO2═Na2CO3+H2O;Na2CO3+CaCl2═CaCO3↓+2NaCl.
分析实验现象并结合所学知识可以得出该固体酒精中的氢氧化钠已经变质.
(3)为进一步确定该固体酒精中氢氧化钠的变质程度,同学们进行了分组探究:
①甲组取(2)中烧杯里的上层清液于洁净的试管中,滴加酚酞溶液后呈现红色,于是得出结论:样品溶液显碱性,其中的氢氧化钠部分变质.
②乙组认为甲组的实验不能证明溶液中一定含有氢氧化钠,理由是碳酸钠溶液显碱性,能使酚酞试液变红色.他们另取烧杯中的上层清液于洁净的试管中,并加入过量氯化钡溶液充分反应后滴加酚酞溶液,溶液变为红色.由此得到结论:所拿固体酒精样品中的氢氧化钠部分变质.
[实验结论]经充分讨论,大家一致认为乙组的实验方案合理,样品中氢氧化钠已部分变质.
[反思交流]乙组实验中加足量氯化钡溶液的目的是使碳酸钠完全反应.
[拓展应用]要除去氢氧化钠变质后产生的杂质,可选择下列试剂中的AC(填序号)
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液.
分析 [实验探究]
二氧化碳能使澄清石灰水变浑浊;
水蒸气遇冷产生水珠;
氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水;
碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠;
氢氧化钠溶液、碳酸钠溶液都是显碱性的溶液,都能够使酚酞试液变红色;
[反思交流]
氯化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠;
[拓展应用]
氢氧化钡和碳酸钠反应生成碳酸钡沉淀和氢氧化钠,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠.
解答 解:[实验探究]
(1)按如图实验,若观察到烧杯内壁有白色固体生成,便可得出酒精燃烧产物中含有二氧化碳,从而得出酒精中含有碳元素;
只要将所用烧杯更换为冷而干燥的烧杯,即可证明燃烧产物中有水蒸汽,从而得出酒精中含有氢元素.
故填:含有碳元素和氢元素.
(2)该白色沉淀的产生途径是:氢氧化钠和空气中的二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O,Na2CO3+CaCl2═CaCO3↓+2NaCl.
故填:2NaOH+CO2═Na2CO3+H2O;Na2CO3+CaCl2═CaCO3↓+2NaCl.
(3)为进一步确定该固体酒精中氢氧化钠的变质程度,同学们进行了分组探究:
②乙组认为甲组的实验不能证明溶液中一定含有氢氧化钠,理由是碳酸钠溶液显碱性,能使酚酞试液变红色.
故填:碳酸钠溶液显碱性,能使酚酞试液变红色.
[反思交流]
乙组实验中加足量氯化钡溶液的目的是使碳酸钠完全反应,防止对检验氢氧化钠产生干扰.
故填:使碳酸钠完全反应.
[拓展应用]
氢氧化钡和碳酸钠反应生成碳酸钡沉淀和氢氧化钠,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,要除去氢氧化钠变质后产生的杂质,可选择下列试剂中的氢氧化钡溶液和氢氧化钙溶液.
故填:AC.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案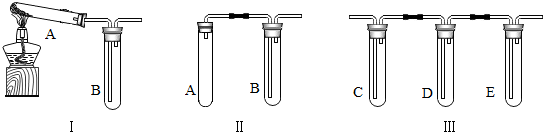
(1)制取气体.
| 气体 | 反应物 | 装置 | 化学方程式 |
| O2 | Ⅰ | ||
| CO2 | 石灰石、稀盐酸 |
(3)探究碳的还原性,将图中的Ⅰ、Ⅲ装置连接,在Ⅰ装置的A试管中加入碳和氧化铜粉末.若反应既有CO2又有CO生成,要证明CO2生成并收集CO,B、D中都加入澄清石灰水,C中加入NaOH溶液,证明有CO2生成的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O,D的作用是检验二氧化碳是否被C中的氢氧化钠溶液完全吸收,E用于收集CO,应对E装置进行的调整是进气管短,出气管要长.
| A. | 将10g锌和10g镁混合加热后,物质的总质量为20g,遵循质量守恒定律 | |
| B. | 化学反应前后原子的总数一定不会发生变化 | |
| C. | 15g木炭和15g氧气完全反应后,生成物质量为30g | |
| D. | 铁丝燃烧后质量增加,不遵循质量守恒定律 |
钠(Na) $\stackrel{O_{2}}{→}$钠的氧化物$\stackrel{H_{2}O}{→}$ 氢氧化钠溶液 $\stackrel{CO_{2}}{→}$白色固体
【提出问题】:常温下钠与氧气反应,产物有哪些?
【查阅资料】:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:
Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2O2,
猜想3:Na2O和Na2O2
【实验探究一】:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | 没有气泡生成 | 猜想1正确 |
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】:
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量白色固体加入足量氯化钙溶液 | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 2.过滤、取少量滤液加入无色的酚酞试液 | 变成红色 |
(1)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为O2.
(3)久置的固体氢氧化钠变质的原因是(用化学方程式表示)2NaOH+CO2═Na2CO3+H2O.
 ”和“
”和“ ”分别表示两种不同质子数的原子,其中可能表示氧化物的是( )
”分别表示两种不同质子数的原子,其中可能表示氧化物的是( )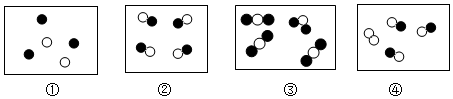
| A. | 只有①④ | B. | ②③④ | C. | 只有② | D. | ①②③④ |
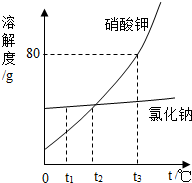 (1)由如图可知,t3℃时,硝酸钾溶解度>氯化钠的溶解度(填“>”,“<”或“=”);
(1)由如图可知,t3℃时,硝酸钾溶解度>氯化钠的溶解度(填“>”,“<”或“=”);