题目内容
10.请结合下列实验常用装置,回答有关问题.
(1)写出图中标有字母的仪器名称:a长颈漏斗.
(2)若用高锰酸钾制取氧气,应选用的发生装置是A(填“A”、“B”或“C”),反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)若要制取二氧化碳,在B装置中装有石灰石,那么a中应加入稀盐酸.若要获得干燥的二氧化碳,除发生装置外,还应选用D装置,并在该装置中盛放浓硫酸(填写试剂名称).如果用E装置收集该气体,则气体从b端进入(填“b”或“c”).
(4)实验室如用块状固体和液体无需加热制取气体,可将B装置改进为C装置(多孔隔板用来放块状固体),其优点是能随时控制反应的开始和终止.
(5)实验室中用锌粒和盐酸反应,制得的氢气混有少量的氯化氢气体和水蒸气,若将B→F→D组装成证明氢气中杂质的装置,则F中装入药品为无水硫酸铜.
(6)硫化氢(H2S)是一种无色、有臭鸡蛋气味的有毒气体,其水溶液叫氢硫酸,具有挥发性.根据上述信息实验室选用如图装置收集硫化氢气体,其中:I装置的作用是防止液体倒吸进H中;J装置的作用是吸收硫酸氢气体,防止污染空气.
分析 (1)熟记仪器的名称;
(2)据反应原理书写方程式,据反应物状态和反应条件选择发生装置;
(3)制取二氧化碳的药品是石灰石和稀盐酸;浓硫酸具有吸水性,可以干燥酸性和中性气体;二氧化碳的密度比空气大,采用向上排空气法收集;
(4)采用隔板,利用气压可以把液体压入长颈漏斗一部分,使固液分离,可以随时控制反应的发生和停止;
(5)根据除杂的顺序来分析;
(6)由题意,“硫化氢(H2S)是一种无色、有臭鸡蛋气味的有毒气体,其水溶液叫氢硫酸,具有挥发性”,所以要进行尾气处理,防止污染空气.
解答 解:(1)a是长颈漏斗;故填:长颈漏斗;
(2)加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,该反应属于固体加热型,故选发生装置A,故填:A;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)制取二氧化碳的药品是石灰石和稀盐酸,石灰石从锥形瓶口加入,稀盐酸从长颈漏斗口加入;干燥二氧化碳用浓硫酸;因为二氧化碳的密度比空气大,所以二氧化碳应该从b管进入,把空气从短管a管排出;故填:稀盐酸;浓硫酸;b;
(4)采用隔板,当关闭开关时,气体排不出去,使试管内的气压增大,利用气压可以把液体压入长颈漏斗一部分,使固液分离,可以控制反应的停止,当打开开关时,固液接触是反应发生,故改进后的优点是:可以随时控制反应的发生.故答案为:能随时控制反应的开始和终止.
(5)实验室中用锌粒和盐酸反应,制得的氢气混有少量的氯化氢气体和水蒸气,检验水蒸气的存在,可在装置F中加入无水硫酸铜粉末,若变蓝色则证明氢气中含有水蒸气;故填:无水硫酸铜;
(6)由题意,可知:I装置的作用是防止液体倒吸进H中、吸收硫化氢气体;J装置的作用是:防止污染空气.故填:防止液体倒吸进H中;吸收硫化氢气体,防止污染空气.
点评 掌握气体制取装置的选取和连接;了解常用仪器的名称和选用;掌握氧气的制取装置的连接和的实验室制法及收集方法.

| A. | 唾液 6.6-7.1 | B. | 胃液 0.9-1.5 | C. | 汗液 6.6-7.6 | D. | 血浆 7.35-7.45 |
| A. | +2 | B. | +3 | C. | +5 | D. | +4 |
(1)若对稀硫酸进行如下操作,溶液的pH升高的有ABC(填字母).
A、加少量水 B、加少量铁粉
C、加少量氢氧化钾 D、加少量浓硫酸
(2)向两个烧杯中分别注入两种硫酸,甲(溶质质量分数为98%,密度为1.84g/cm3)和乙(硫酸甲与水的按体积比1:1混合)个10m,称量并记录不同时间(g)两种硫酸溶液吸水的质量,数据见表:
| 时间/h | 1 | 1.5 | 4 | 8 | 12 | 24 | 48 | 60 | |
| 吸水 质量/g | 硫酸甲 | 1.6 | 2.2 | 5.2 | 10.3 | 14.0 | 20.9 | 29.2 | 32.1 |
| 硫酸乙 | 1.2 | 1.5 | 3.5 | 5.9 | 8.1 | 12.9 | 19.5 | 21.0 | |
②由表中实验数据可知:有关硫酸吸水性的说法错误的是B(填字母).
A.硫酸甲和乙都有吸水性 B.只有硫酸甲有吸水性C.硫酸甲的吸水性较硫酸乙强
(3)小军同学利用稀释后的稀硫酸和硝酸钡、氢氧化钠、碳酸钾等物质的溶液对“复分解反应发生的条件”进行再探究.
①将上述四种溶液两两混合,判断其两两之间能否发生反应,请写出其中发生中和反应的化学方程H2SO4+2NaOH═Na2SO4+2H2O.
②利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液.经测定,该溶液显酸性.则在该溶液中一定含有的离子是H+、Na+、K+和NO3-,可能含有的离子是SO42-.
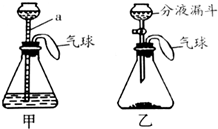 某化学兴趣小组设计了一组“吹气球”实验,两套装置如图所示:
某化学兴趣小组设计了一组“吹气球”实验,两套装置如图所示:
 某兴趣小组利用如图所示装置测定石灰石样品中碳酸钙的质量分数,探究过程如下(注:石灰石样品中的杂质不参与反应也不溶解);
某兴趣小组利用如图所示装置测定石灰石样品中碳酸钙的质量分数,探究过程如下(注:石灰石样品中的杂质不参与反应也不溶解);