题目内容
1.分析如图,回答下列问题.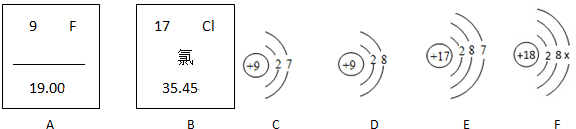
(1)D、E、F三种粒子的结构示意图中,与C属于同种元素的粒子是D (填字母代号).
(2)在C、D、E、F四种粒子的结构示意图中C和E(填字母代号)元素的化学性质相似;得到电子的是D(填字母代号),形成的是阴(填“阴”或“阳”)离子;
填写A粒子中的横线为氟;F原子结构示意图中X数值为8.
(3)用化学符号写出氟离子:F-,2个氟原子2F,氟气F2.
分析 (1)元素是质子数(即核电荷数)相同的一类原子的总称,同种元素的粒子是质子数相同,据此进行分析解答;
(2)根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,决定元素种类的是核电荷数(即核内质子数),根据元素的化学性质跟它的原子的最外层电子数目有关,决定元素的化学性质的是原子的最外层电子数,据此进行分析解答;核电荷数=质子数=电子数;
(3)本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:(1)元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),同种元素的粒子是质子数相同,CD的质子数相同,属于同种元素;
(2)根据决定元素种类的是核电荷数(即核内质子数),因为B、C的核内质子数相同,所以B、D属于同种元素的粒子;决定元素的化学性质的是原子的最外层电子数,C子D子的最外层电子数相同,C粒子化学性质与D粒子化学性质相似.最容易得到电子的是D,形成阴离子;A是氟元素,因在原子结构示意图,核内质子数=核外电子数,故乙中X=18-2-8=8;
(3)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,氟离子表示为:F-
原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.所以2个氟原子,就可表示为:2F
氟气属于气态非金属单质,在元素符号的右下角写上表示分子中所含原子数的数字,其化学式为:F2
点评 本题考查学生对元素的种类由质子数决定、原子结构示意图的特点在解题中灵活应用的能力.

 同步奥数系列答案
同步奥数系列答案| A. | 纯净物一定是由分子构成的 | |
| B. | 由同种分子构成的物质一定是纯净物 | |
| C. | 混合物肯定是由两种以上的元素组成 | |
| D. | 硫酸(H2SO4)是2个氢元素,1个硫元素,4个氧元素构成 |
| A. | 一定有碳酸钠 | B. | 可能有氢氧化钠 | C. | 一定有碳酸钙 | D. | 可能有氢氧化钙 |

 (1)将含有蔗糖晶体的溶液A.从冰箱里取出放置一段时间后,晶体慢慢消失,形成溶液B.对于溶液A和B,一定处于饱和状态的是的是A.其中溶质质量分数较大的是B.
(1)将含有蔗糖晶体的溶液A.从冰箱里取出放置一段时间后,晶体慢慢消失,形成溶液B.对于溶液A和B,一定处于饱和状态的是的是A.其中溶质质量分数较大的是B.