题目内容
4.实验室用已配置好的质量分数为6%的氯化钠溶液(密度约为1.04g/cm3),配制50g质量分数为3%的氯化钠溶液.(1)配制步骤为:计算、量取、混匀.
(2)需要6%的氯化钠溶液24mL.(结果取整数)
(3)某同学在量取6%的氯化钠溶液体积时俯视读数,则实际配制溶液的溶质质量分数将偏小.(填“偏大”、“偏小”或“不变”)
分析 (1)根据用浓溶液配制溶质质量分数一定的稀溶液的基本步骤进行分析解答.
(2)根据溶液稀释前后,溶质的质量不变,结合题意进行分析解答.
(3)量取6%的氯化钠溶液体积时俯视读数,读数比实际液体体积大,会造成实际量取的氯化钠溶液的体积偏小,据此进行分析解答.
解答 解:(1)已配制好的质量分数为6%的氯化钠溶液(密度约为1.04g/cm3)配制50g质量分数为3%的氯化钠溶液,首先计算配制溶液所需6%的氯化钠溶液的质量,再量取所需的氯化钠溶液和量取水,最后进行溶解混匀.
(2)设需要6%的氯化钠溶液的体积为x,根据溶液稀释前后,溶质的质量不变,
则50g×3%=1.04g/cm3×x×6% x=24cm3=24mL.
(3)量取6%的氯化钠溶液体积时俯视读数,读数比实际液体体积大,会造成实际量取的氯化钠溶液的体积偏小,则实际配制溶液的溶质质量分数将偏小.
故答案为:(1)量取;(2)24;(3)偏小.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、注意事项等是正确解答本题的关键.

练习册系列答案
相关题目
14.在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表.则关于此反应的认识正确的是( )
| 物质 | X | Y | Z | W |
| 反应前的质量(g) | 2 | 1 | 16 | 16 |
| 反应后的质量(g) | 17 | m | 6 | 11 |
| A. | 该反应用化学方程式表示为:3X+Y=2Z+W | |
| B. | 该反应的基本类型为化合反应 | |
| C. | m=2 | |
| D. | 反应后容器中Z与Y的质量比为1:6 |
15.现有10.6g碳酸钠和8.4g碳酸氢钠,分别与过量盐酸反应,其中( )
| A. | 碳酸钠消耗的氯化氢多 | B. | 碳酸氢钠生成的二氧化碳多 | ||
| C. | 碳酸氢钠消耗的氯化氢多 | D. | 碳酸氢钠生成的二氧化碳多 |
16.下列现象中,只发生物理变化的是( )
| A. | 玻璃破碎 | B. | 牛奶变质 | C. | 木炭燃烧 | D. | 粮食酿酒 |
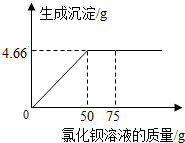 将4g含有可溶性杂质的硫酸铜样品溶于足量水,再向所得溶液中逐渐滴加75g一定溶质质量分数的氯化钡溶液(杂质不与氯化钡溶液反应),实验过程中,生成沉淀的质量与滴入氯化钡溶液的质量关系如图所示.试计算:
将4g含有可溶性杂质的硫酸铜样品溶于足量水,再向所得溶液中逐渐滴加75g一定溶质质量分数的氯化钡溶液(杂质不与氯化钡溶液反应),实验过程中,生成沉淀的质量与滴入氯化钡溶液的质量关系如图所示.试计算: