题目内容
8.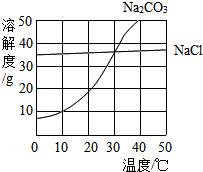 图为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线.
图为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线.(1)当温度为30℃时,两种物质的溶解度有什么关系?
(2)生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”.请你解释原因:
“夏天晒盐”“冬天捞碱”
分析 从图中可以看出氯化钠的溶解度受温度变化影响不大,所以在改变温度时,氯化钠在水中的溶解能力基本保持不变.而碳酸钠的溶解度受温度变化影响较大,所以在改变温度时,碳酸钠在水中的溶解能力会发生较大的改变.
解答 解:从溶解度曲线图中可以看出在温度等于30℃时,氯化钠的溶解度与碳酸钠的溶解度相同.同时也能看出碳酸钠的溶解度受温度影响较大,当温度升高时,溶解度升高,所以在夏天,虽然水分蒸发但碳酸钠的溶解能力变大,碳酸钠不析出.冬天时温度降低碳酸钠析出.而氯化钠的溶解度受温度影响较小,所以在夏天时,虽然温度升高了,但水分少了,所以氯化钠析出.而冬天时,温度虽然降低,但氯化钠的溶解能力变化不大,所以没有析出.
故答案为:(1)当温度为30℃时,氯化钠的溶解度与碳酸钠的溶解度相同.
(2)氯化钠的溶解度受温度影响不大,夏天温度高水分蒸发快,氯化钠易结晶析出;碳酸钠的溶解度受温度影响大,夏天温度高,溶解能力变大,冬天温度低,碳酸钠易结晶析出,而氯化钠的溶解能力变化小不析出;所以“夏天晒盐”“冬天捞碱”.
点评 氯化钠的溶解度受温度影响较小,所以在夏天时温度虽然升高,溶解能力变化小,但水分挥发所以氯化钠析出.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.为除去粗盐中不溶性杂质,下列操作合理的是( )
| A. | 粗盐研细是为了增大食盐的溶解度 | |
| B. | 过滤时液体的液面要低于滤纸边缘 | |
| C. | 加热蒸发时不断搅拌直至水分全部蒸干 | |
| D. | 实验结束随即将蒸发皿取下放在桌面上 |
18.向100g含氢氧化钠和碳酸钠的混合溶液中加入50g质量分数为7.3%的稀盐酸,恰好完全反应得到中性溶液,则蒸干该溶液可得到的质量为( )
| A. | 5.85g | B. | 11.7g | C. | 17.55g | D. | 160.3g |
16.下列属于化学变化的是( )
| A. | 食物腐烂 | B. | 干冰升华 | C. | 酒精挥发 | D. | 矿石粉碎 |
13.下表是氯化钠和硝酸钾在不同温度下的溶解度数据,根据数据回答问题.
(1)由数据知,氯化钠属于易溶(填易溶、可溶、微溶或难溶)物质.溶解度受温度影响变化比较大的物质是KNO3(填“NaCl”或“KNO3”).
(2)从NaCl的饱和溶液中提取NaCl,应采用的方法是Ⅱ(填序号).
Ⅰ.冷却结晶Ⅱ.蒸发溶剂Ⅲ.过滤
(3)20℃时,把17克氯化钠和17克硝酸钾分别放入50克水中,能形成饱和溶液且其饱和溶液的质量是65.8克.为使其变为不饱和溶液,可采用的一种方法是加水.
(4)根据数据分析,氯化钠和硝酸钾的溶解度相等的温度范围是Ⅱ(填序号).
I.0℃~20℃Ⅱ.20℃~40℃Ⅲ.40℃~60℃Ⅳ. 60℃~80℃
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g/100g水) | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
(2)从NaCl的饱和溶液中提取NaCl,应采用的方法是Ⅱ(填序号).
Ⅰ.冷却结晶Ⅱ.蒸发溶剂Ⅲ.过滤
(3)20℃时,把17克氯化钠和17克硝酸钾分别放入50克水中,能形成饱和溶液且其饱和溶液的质量是65.8克.为使其变为不饱和溶液,可采用的一种方法是加水.
(4)根据数据分析,氯化钠和硝酸钾的溶解度相等的温度范围是Ⅱ(填序号).
I.0℃~20℃Ⅱ.20℃~40℃Ⅲ.40℃~60℃Ⅳ. 60℃~80℃
17.日本海啸引发的核爆炸,使得“碘”成为备受世人关注的焦点.实验室从海藻中提取碘,有如下化学反应:2NaI+Cl2═2NaCl+I2,这一反应所属类型是( )
| A. | 复分解反应 | B. | 化合反应 | C. | 置换反应 | D. | 分解反应 |
18.用分子观点解释如图漫画中小女孩的话,正确的是( )


| A. | 分子质量小 | B. | 分子在不断地运动 | ||
| C. | 分子体积小 | D. | 分子间有间隔 |
