题目内容
2.某温度时,将6g氯化钾完全溶于24g水中.(1)求该溶液中溶质的质量分数20%.
(2)若要使溶液中溶质质量分数增大到25%,则需加多少克溶质或蒸发多少克溶剂?
分析 利用溶液中溶质质量分数的定义,溶液中溶质的质量分数=$\frac{溶质的质量}{溶液的质量}$,计算该溶液中溶质的质量分数.
要使溶液的溶质质量分数变大,常通过两种方式:①加入溶质,②蒸发溶剂,据此结合溶质质量分数的计算进行分析解答.
解答 解:(1)该溶液中溶质的质量分数=$\frac{6g}{6g+24g}×100%$=20%
答案:20%;
(2)设需要再溶解该物质的质量为x,(6g+24g+x)×25%=(6g+24g)×20%+x,x=2g.
设需要蒸发水的质量为y,(6g+24g-y)×25%=(6g+24g)×20%,y=6g.
故答案为:若要使溶液中溶质质量分数增大到25%,则需加2克溶质或蒸发6克水.
点评 本题难度不大,掌握溶液中溶质的质量分数=$\frac{溶质的质量}{溶液的质量}$,是正确解答本题的关键.

练习册系列答案
相关题目
10.下列关于溶液的说法正确的是( )
| A. | 同种固态溶质的饱和溶液的溶质的质量分数一定比不饱和溶液的溶质的质量分数大 | |
| B. | 在某固态物质的饱和溶液里加入其他任何物质都不能溶解 | |
| C. | 某固态物质的饱和溶液,当温度升高时,若溶液质量不变,则溶质的质量分数不变 | |
| D. | 温度升高,KNO3的饱和溶液就变成不饱和溶液,所以溶液的溶质的质量分数也随之而减少 |
13.将40g10%的硝酸钾溶液变成20%的溶液,可采用的方法是( )
| A. | 蒸发掉溶剂的一半 | B. | 再加入40g10%的硝酸钾溶液 | ||
| C. | 再加入4g硝酸钾 | D. | 蒸发浓缩成20g硝酸钾溶液 |
10.加碘食盐包装袋上的“含碘量”中“碘”指的是( )
| A. | 原子 | B. | 元素 | C. | 分子 | D. | 电子 |
7.新修订的《环境质量标准》增加了PM2.5监测指标,PM2.5是指大气中直径小于或等于2.5μm的可吸入颗粒物.下列做法不会改变PM2.5监测结果的是( )
| A. | 燃放鞭炮 | B. | 河水蒸发 | C. | 露天焚烧秸秆 | D. | 工厂排放烟尘 |
14.雄伟壮观的国家大剧院主体建筑表面安装了近2万块钛(Ti)金属板.已知Ti原子核内有22个质子,则下列叙述正确的是( )
| A. | Ti可以表示一个钛原子 | B. | Ti4+核外有26个电子 | ||
| C. | TiO2中含有氧分子 | D. | Ti4+表示钛元素显+4价 |
11.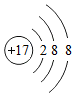 如图所示是氯离子的结构示意图,下列说法正确的是( )
如图所示是氯离子的结构示意图,下列说法正确的是( )
 如图所示是氯离子的结构示意图,下列说法正确的是( )
如图所示是氯离子的结构示意图,下列说法正确的是( )| A. | 氯是金属元素 | B. | 氯离子最外电子层已达到稳定结构 | ||
| C. | 氯离子的核电荷数为18 | D. | 氯离子的符号是Cl+ |