题目内容
3.生活中的科学.初二年级去社会生产实践时,同学们做蛋糕时都要用到纯碱,它的化学式是Na2CO3.
分析 纯碱是碳酸钠的俗称,钠元素显+1价,碳酸根显-2价,写出其化学式即可.
解答 解:纯碱是碳酸钠的俗称,钠元素显+1价,碳酸根显-2价,其化学式为:Na2CO3.
故答案为:Na2CO3.
点评 本题难度不大,掌握化合物化学式的书写一般规律(金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零)是正确解答此类题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.下列物质暴露在空气中一段时间其质量会增加且发生化学变化的是( )
| A. | 浓盐酸 | B. | 浓硫酸 | C. | 无水CuSO4 | D. | 生石灰 |
18.根据化学实验常识,判断下列事故处理方法正确的是( )
| A. | 炒菜时油锅着火,立即盖上锅盖 | |
| B. | 发现煤气泄漏时,立即打开排风扇开关 | |
| C. | 高层住房着火时,立即打开所有门窗 | |
| D. | 家用电器着火时,立即用水浇灭 |
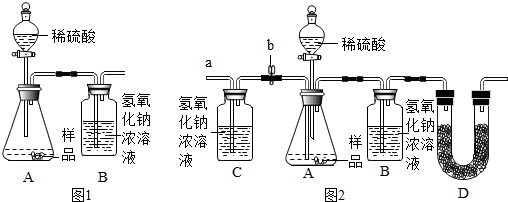
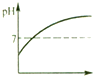
8.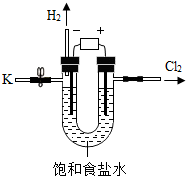 某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.
某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.
老师提示:
Ⅰ.电解饱和食盐水的化学方程式:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ 2NaOH+H2↑+Cl2↑
Ⅱ.忽略其他可能发生的反应对本实验的影响.
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,确定待测液中含有氢氧化钠.
探究活动二:测定待测液中氢氧化钠的质量分数
【实验1】用酸碱中和法测定
甲组同学称取一定质量的待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加入
一定溶质质量分数的稀盐酸,边加边振荡,用pH计测定溶液的pH,所得数据如下:
(2)利用氢氧化钠与稀盐酸恰好完全反应时的实验数据计算所称取待测液中氢氧化钠的质量时,应选用稀盐酸的体积为9.8mL.
【实验2】用沉淀法测定
资料摘要:氢氧化钠与氯化镁在溶液中发生反应:2NaOH+MgCl2=Mg(OH)2↓+2NaCl.
乙组同学按下图所示的实验步骤进行实验:
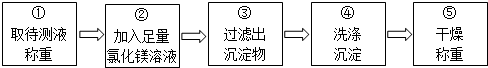
(3)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.
(4)步骤③过滤出的沉淀物是氢氧化镁.
(5)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
 某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.
某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.老师提示:
Ⅰ.电解饱和食盐水的化学方程式:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ 2NaOH+H2↑+Cl2↑
Ⅱ.忽略其他可能发生的反应对本实验的影响.
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,确定待测液中含有氢氧化钠.
探究活动二:测定待测液中氢氧化钠的质量分数
【实验1】用酸碱中和法测定
甲组同学称取一定质量的待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加入
一定溶质质量分数的稀盐酸,边加边振荡,用pH计测定溶液的pH,所得数据如下:
| 加入稀盐酸的体积/mL | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 9.8 |
| 烧杯中溶液的pH | 13.0 | 12.9 | 12.8 | 12.6 | 12.3 | 7.0 |
【实验2】用沉淀法测定
资料摘要:氢氧化钠与氯化镁在溶液中发生反应:2NaOH+MgCl2=Mg(OH)2↓+2NaCl.
乙组同学按下图所示的实验步骤进行实验:

(3)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.
(4)步骤③过滤出的沉淀物是氢氧化镁.
(5)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
13.有三瓶无色气体,分别是空气,氧气,二氧化碳,下列方法能一次性正确鉴别的是( )
| A. | 带火星的木条 | B. | 澄清的石灰水 | C. | 燃着的木条 | D. | 闻气味 |