题目内容
如图装置可以用来制取O2、CO2、H2等,请回答有关问题.
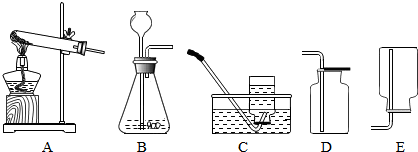
(1)用过氧化氢溶液和二氧化锰来制取氧气的发生装置是 (填编号,下同),收集装置是 ,反应的化学方程式为 ,其中二氧化锰起 作用.
(2)用高锰酸钾制取氧气的化学方程式为 ,可选用 发生装置;进行实验时,试管口应 ,以防止加热时高锰酸钾粉末进入导管.用高锰酸钾制取并用排水法收集氧气有以下操作步骤:①加热 ②熄灭酒精灯 ③检验装置气密性 ④装入药品 ⑤收集氧气 ⑥从水中撤出导管 ⑦用铁架台固定装置.正确的操作顺序为 .用高锰酸钾制取氧气,试管口要略向下倾斜,原因是 .加热前要先预热,方法是 ,目的是 .
(3)用氯酸钾和二氧化锰来制取和收集氧气的装置组合是 和 ,反应的化学方程式为 .若用排水法收集氧气完毕,应先 、后 ,原因是 .
(4)实验室制取二氧化碳的药品是(填名称) ,反应的化学方程式是 .应选用的发生装置是 ,依据是 、 ;应选用的收集装置是 .依据是 、 .把产生的二氧化碳通入紫色石蕊试液中发生的现象是 ,原因是(用化学方程式表示) ;把上述的溶液加热后发生的现象是 ,原因是(用化学方程式表示): .
(5)实验室用锌粒和稀硫酸溶液发生反应(无需加热)来制取氢气,制取和收集氢气的装置组合是 和 ;在点燃氢气前,必须要做的工作是 .

(1)用过氧化氢溶液和二氧化锰来制取氧气的发生装置是
(2)用高锰酸钾制取氧气的化学方程式为
(3)用氯酸钾和二氧化锰来制取和收集氧气的装置组合是
(4)实验室制取二氧化碳的药品是(填名称)
(5)实验室用锌粒和稀硫酸溶液发生反应(无需加热)来制取氢气,制取和收集氢气的装置组合是
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,制取氧气的操作步骤和注意点,二氧化碳的实验室制法,二氧化碳的化学性质,氢气的制取和检验,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
氧气不易溶于水,密度比空气大;
(2)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气;
利用加热的方法制取气体,并且用排水法收集时,要按照一定的步骤进行,特别是要注意集满气体后的操作顺序,以防发生安全事故;
(3)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;
(4)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石和石灰石的主要成分是碳酸钙,通常情况下,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳能够溶于水,密度比空气大;
二氧化碳能和水反应生成碳酸,碳酸在加热条件下分解生成水和二氧化碳;
(5)根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置.
氧气不易溶于水,密度比空气大;
(2)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气;
利用加热的方法制取气体,并且用排水法收集时,要按照一定的步骤进行,特别是要注意集满气体后的操作顺序,以防发生安全事故;
(3)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;
(4)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石和石灰石的主要成分是碳酸钙,通常情况下,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳能够溶于水,密度比空气大;
二氧化碳能和水反应生成碳酸,碳酸在加热条件下分解生成水和二氧化碳;
(5)根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置.
解答:解:(1)用过氧化氢溶液和二氧化锰来制取氧气时不需要加热,发生装置应该用B装置;
因为氧气的密度比空气大,可以用向上排空气法收集,即用D装置收集,氧气不易溶于水,可以用排水法收集,即用C装置收集;
反应的化学方程式为:2H2O2
2H2O+O2↑,其中二氧化锰起催化作用.
故填:B;C或D;2H2O2
2H2O+O2↑;催化.
(2)用高锰酸钾制取氧气的化学方程式为:2KMnO4
K2MnO4+MnO2+O2↑;
因为反应需要加热,应该选用A装置作为发生装置;
进行实验时,试管口应塞一团棉花,以防止加热时高锰酸钾粉末进入导管;
用高锰酸钾制取并用排水法收集氧气时,应该先检验装置气密性,再装入药品,再用铁架台固定装置,再加热,再收集氧气,再从水中撤出导管,最后熄灭酒精灯,即顺序为③④⑦①⑤⑥②;
用高锰酸钾制取氧气,试管口要略向下倾斜,原因是能够防止水蒸气冷凝、回流炸裂试管;
加热前要先预热,方法是移动酒精灯在试管下方来回加热,目的是使试管均匀受热,防止炸裂.
故填:2KMnO4
K2MnO4+MnO2+O2↑;A;塞一团棉花;③④⑦①⑤⑥②;防止水蒸气冷凝、回流炸裂试管;移动酒精灯在试管下方来回加热;使试管均匀受热,防止炸裂.
(3)用氯酸钾和二氧化锰来制取和收集氧气的装置组合是 A和 C或D,反应的化学方程式为 2KClO3
2KCl+3O2↑.若用排水法收集氧气完毕,应先 把导管移出水面、后 熄灭酒精灯,原因是 防止水倒流入试管,把试管炸裂.
故填:A;C或D;2KClO3
2KCl+3O2↑;把导管移出水面;熄灭酒精灯;防止水倒流入试管,把试管炸裂.
(4)实验室制取二氧化碳的药品是大理石或石灰石和稀盐酸,反应的化学方程式是:
CaCO3+2HCl═CaCl2+H2O+CO2↑;
因为反应不需要加热,应选用的发生装置是B装置,依据是:反应物是固体和液体、不需要加热;
应选用的收集装置是D,依据是:密度比空气大、不和空气中的物质反应;
把产生的二氧化碳通入紫色石蕊试液中发生的现象是:紫色石蕊试液变红色,原因是:二氧化碳和水反应生成碳酸,碳酸能使石蕊试液变红色,反应的化学方程式为:H2O+CO2═H2CO3;
把上述的溶液加热后发生的现象是:溶液由红色变成紫色,原因是:碳酸受热分解生成水和二氧化碳,反应的化学方程式为:H2CO3
H2O+CO2↑.
故填:大理石或石灰石和稀盐酸;CaCO3+2HCl═CaCl2+H2O+CO2↑;B;反应物是固体和液体;不需要加热;D;密度比空气大;不和空气中的物质反应;紫色石蕊试液变红色;H2O+CO2═H2CO3;溶液由红色变成紫色;H2CO3
H2O+CO2↑.
(5)实验室用锌粒和稀硫酸溶液发生反应来制取氢气时不需要加热,应该用B装置作为发生装置;
氢气不溶于水,可以用排水法收集,即用C装置收集,密度比空气小,可以用向下排空气法收集,即用E装置收集;
因为氢气与氧气或空气混合时遇明火可能会发生爆炸,因此在点燃氢气前,必须要检验氢气的纯度.
故填:B;C或E;验纯.
因为氧气的密度比空气大,可以用向上排空气法收集,即用D装置收集,氧气不易溶于水,可以用排水法收集,即用C装置收集;
反应的化学方程式为:2H2O2
| ||
故填:B;C或D;2H2O2
| ||
(2)用高锰酸钾制取氧气的化学方程式为:2KMnO4
| ||
因为反应需要加热,应该选用A装置作为发生装置;
进行实验时,试管口应塞一团棉花,以防止加热时高锰酸钾粉末进入导管;
用高锰酸钾制取并用排水法收集氧气时,应该先检验装置气密性,再装入药品,再用铁架台固定装置,再加热,再收集氧气,再从水中撤出导管,最后熄灭酒精灯,即顺序为③④⑦①⑤⑥②;
用高锰酸钾制取氧气,试管口要略向下倾斜,原因是能够防止水蒸气冷凝、回流炸裂试管;
加热前要先预热,方法是移动酒精灯在试管下方来回加热,目的是使试管均匀受热,防止炸裂.
故填:2KMnO4
| ||
(3)用氯酸钾和二氧化锰来制取和收集氧气的装置组合是 A和 C或D,反应的化学方程式为 2KClO3
| ||
| △ |
故填:A;C或D;2KClO3
| ||
| △ |
(4)实验室制取二氧化碳的药品是大理石或石灰石和稀盐酸,反应的化学方程式是:
CaCO3+2HCl═CaCl2+H2O+CO2↑;
因为反应不需要加热,应选用的发生装置是B装置,依据是:反应物是固体和液体、不需要加热;
应选用的收集装置是D,依据是:密度比空气大、不和空气中的物质反应;
把产生的二氧化碳通入紫色石蕊试液中发生的现象是:紫色石蕊试液变红色,原因是:二氧化碳和水反应生成碳酸,碳酸能使石蕊试液变红色,反应的化学方程式为:H2O+CO2═H2CO3;
把上述的溶液加热后发生的现象是:溶液由红色变成紫色,原因是:碳酸受热分解生成水和二氧化碳,反应的化学方程式为:H2CO3
| ||
故填:大理石或石灰石和稀盐酸;CaCO3+2HCl═CaCl2+H2O+CO2↑;B;反应物是固体和液体;不需要加热;D;密度比空气大;不和空气中的物质反应;紫色石蕊试液变红色;H2O+CO2═H2CO3;溶液由红色变成紫色;H2CO3
| ||
(5)实验室用锌粒和稀硫酸溶液发生反应来制取氢气时不需要加热,应该用B装置作为发生装置;
氢气不溶于水,可以用排水法收集,即用C装置收集,密度比空气小,可以用向下排空气法收集,即用E装置收集;
因为氢气与氧气或空气混合时遇明火可能会发生爆炸,因此在点燃氢气前,必须要检验氢气的纯度.
故填:B;C或E;验纯.
点评:实验是化学的重要组成部分,正确的实验操作是得出科学结论的前提条件之一,因此要学会设计实验、进行实验、分析实验,为得出正确的结论奠定基础.

练习册系列答案
相关题目
某化学反应可以用微观示意图表示(如图),下列有关说法正确的是( )

| A、该反应前后分子的种类不变 |
| B、示意图中虚线框内的原子应该是“O” |
| C、该反应涉及到四种原子 |
| D、参与反应的物质其类别都是化合物 |

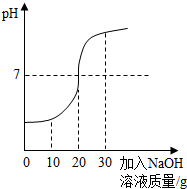 化学兴趣小组对某工业废水(含有H2SO4、Na2SO4)中H2SO4的含量进行测定.甲、乙两同学各提出不同的测定方法,请回答有关问题:
化学兴趣小组对某工业废水(含有H2SO4、Na2SO4)中H2SO4的含量进行测定.甲、乙两同学各提出不同的测定方法,请回答有关问题: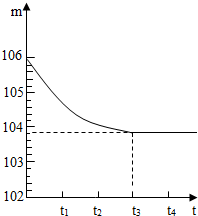 我县蕴含丰富的石灰石资源,小欣同学在山上采集了一块石灰石样品,想测定石灰石中碳酸钙的含量.小欣与同学们讨论后得出以下方案.
我县蕴含丰富的石灰石资源,小欣同学在山上采集了一块石灰石样品,想测定石灰石中碳酸钙的含量.小欣与同学们讨论后得出以下方案. 2010年3月22日是第十八届“世界水日”,联合国确定的2010年“世界水日”主题是“关注水质、抓住机遇、应对挑战”.水是生命之源,为了人类和社会经济的可持续发展,我们必须爱护水资源,一方面要节约用水,另一方面要防止水体污染.
2010年3月22日是第十八届“世界水日”,联合国确定的2010年“世界水日”主题是“关注水质、抓住机遇、应对挑战”.水是生命之源,为了人类和社会经济的可持续发展,我们必须爱护水资源,一方面要节约用水,另一方面要防止水体污染.