题目内容
9.氯酸钾在二氧化锰作催化剂并加热的条件下,分解生成氯化钾和氧气.把干燥纯净的氯酸钾与二氧化锰的混合物15g装入大试管中加热,待反应不再发生,试管冷却后,称得固体质量为10.2g,试计算:(1)制得氧气的质量为:4.8g
(2)原混合物中氯酸钾与二氧化锰的质量各是多少克?
分析 (1)根据质量守恒定律计算生成氧气的质量;
(2)根据生成氧气的质量化学方程式进行计算.
解答 解:(1)生成氧气的质量为:15g-10.2g=4.8g;
(2)设混合物中氯酸钾的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 4.8g
$\frac{245}{x}$=$\frac{96}{4.8g}$
x=12.25g
二氧化锰的质量为15g-12.25g=2.75g
故答案为:(1)4.8g;
(2)原混合物中氯酸钾与二氧化锰的质量各是12.25g,2.75g.
点评 本题主要考查学生运用化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.化学反应的程度与反应物的浓度之间有一定的规律可循.某实验小组各取等量的木炭和等质量的硫分别在容积相同的集气瓶中燃烧.记录如表:
通过A、B两组对比实验的现象,可以得出的规律是:可燃物在氧气中燃烧比在空气中燃烧要剧烈.
| 实验 | 实验步骤 | 实验现象 | 燃烧反应的文字表达式 | |
| A | ①木炭在空气中燃烧 | ①木炭红热 | 产生的气体都能使澄清石灰水变浑浊 | 碳+氧气$\stackrel{点燃}{→}$二氧化碳 |
| ②木炭在氧气中燃烧 | ②发出白光,放热 | |||
| B | ③硫在空气中燃烧 | ③微弱的淡蓝色火焰 | 产生的气体都有刺激性气味 | 硫+氧气$\stackrel{点燃}{→}$二氧化硫 |
| ④硫在氧气中燃烧 | ④明亮的蓝紫色火焰,放热 | |||
4.已知硝酸钾在20℃时的溶解度是31.6克,如果要改变硝酸钾的溶解度,可行的是( )
| A. | 改变溶剂的量 | B. | 改变温度 | ||
| C. | 改变搅拌的速度 | D. | 改变硝酸钾的颗粒大小 |
19.央视2016年3.15主题是“新消费•我做主”,曝光了很多与食品相关的问题,下列做法正确的是( )
| A. | 用鱼粉、工业明胶合成鱼翅 | B. | 白酒中加入超量塑化剂使口感更好 | ||
| C. | 在排骨汤中放入食用碘盐调味 | D. | 鸡饲料中添加各种抗生素使鸡速成 |
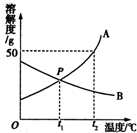 图是A、B两种固体物质的溶解度曲线.
图是A、B两种固体物质的溶解度曲线.