题目内容
14.为测定某Cu-Zn合金中铜的质量分数,某同学将20g该合金放入到盛有100g溶质质量分数为9.8%稀硫酸的烧杯中,恰好完全反应.计算原合金中铜的质量分数.分析 铜不与稀硫酸反应,依据反应的硫酸的质量利用方程式可求反应的锌的质量,从而求出该黄铜样品中铜的质量分数;
解答 解:铜不与稀硫酸反应,
设样品中锌的质量是x
Zn+H2SO4=ZnSO4+H2↑
65 98
x 100g×9.8%
$\frac{65}{x}=\frac{98}{100g×9.8%}$
x=6.5g
该黄铜样品中铜的质量分数=$\frac{20g-6.5g}{20g}$×100%=67.5%
答案:该黄铜样品中铜的质量分数为67.5%.
点评 本题考查根据化学方程式的简单计算,已知生成物的质量求反应物的质量.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案
相关题目
2.生活中的下列变化,只发生物理变化的是( )
| A. | 铁器生锈 | B. | 香水挥发 | C. | 蜡烛燃烧 | D. | 食物腐败 |
9.下列关于氧气的化学性质的说法中,正确的是( )
| A. | 氧气不易溶于水 | B. | 氧气具有可燃性 | C. | 化学性质不活泼 | D. | 具有氧化性 |
4.下列按酸、碱、盐的顺序排列的一组是( )
| A. | H2SO4 NaHCO3 NaCl | B. | Ca(OH)2 HCl Na2SO4 | ||
| C. | NaOH HNO3 NaCl | D. | H2CO3 NaOH NaHCO3 |
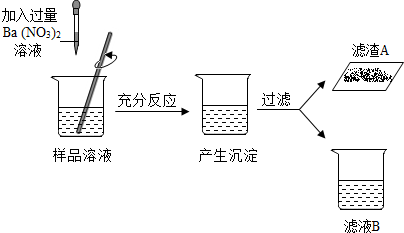


 现有 A、B、C、D、E五种溶液,它们分別是氢氧化钠的溶液、硫酸铜溶液、碳酸钠溶液、.氯化钠溶液和稀硫酸中的一种,鉴别它们可按如图所示的步骤进行.
现有 A、B、C、D、E五种溶液,它们分別是氢氧化钠的溶液、硫酸铜溶液、碳酸钠溶液、.氯化钠溶液和稀硫酸中的一种,鉴别它们可按如图所示的步骤进行.