题目内容
兴趣小组的同学研究(Cu﹣Zn合金)样品中锌的含量,取该样品18g跟足量的稀硫酸充分反应,产生氢气的质量与所用稀硫酸的质量关系如图所示.请计算:
(1)18g该样品中锌的质量.
(2)稀硫酸中溶质的质量分数.
| 根据化学反应方程式的计算;有关溶质质量分数的简单计算. | |
| 专题: | 综合计算(图像型、表格型、情景型计算题). |
| 分析: | Cu﹣Zn合金中锌的活动性比氢强,能与稀硫酸反应,铜不能;由产生氢气的质量与所用稀硫酸的质量关系图可知,该样品18g跟足量的稀硫酸充分反应,产生氢气的质量为0.2g,恰好完全反应消耗的稀硫酸的质量为100g,据此由锌和稀硫酸反应的化学方程式,进行分析解答. |
| 解答: | 解:该样品18g跟足量的稀硫酸充分反应,产生氢气的质量为0.2g. 设18g该样品中锌的质量为x,稀硫酸中溶质的质量为y, Zn+H2SO4=ZnSO4+H2↑ 65 98 2 x y 0.2g (1) (2) 稀硫酸中溶质的质量分数为 答:(1)18g该样品中锌的质量为6.5g;(2)稀硫酸中溶质的质量分数为9.8%. |
| 点评: | 本题难度较大,主要考查学生根据图表数据、化学方程式的计算进行解决问题的能力,由关系图确定产生氢气的质量是正确解答本题的关键. |

下列四个坐标示意图分别表示四个实验过程中的某些变化情况,其中错误的是( )
|
| A. |
加热一定量碳铵(NH4HCO3)的实验,试管中固体的质量变化 |
|
| B. |
等质量的镁条和铁丝分别与足量的稀硫酸反应,产生气体的质量变化 |
|
| C. |
向一定量的二氧化锰固体中加入一定量的过氧化氢溶液,二氧化锰的质量变化 |
|
| D. |
将水通电一段时间,相同状况下产生气体的体积变化 |
下列实验对应现象的描述错误的是( )
|
| A. |
铁丝在氧气中燃烧:剧烈燃烧,火星四射,放出大量的热.产生黑色固体 |
|
| B. |
一氧化碳在高温条件下还原氧化铁:试管中红色固体变成黑色,澄清的石灰水变浑浊 |
|
| C. |
电解水的实验:两个电极上产生大量的气泡,正极上产生的是氢气,负极上产生的是氧气 |
|
| D. |
测定空气成分的实验:玻璃管内红色的固体粉末变成黑色,气体的总体积减少了约 |
某同学设计了以下三个实验,要证明Cu、Zn、Ag的活动性顺序,必须要做的实验是( )
|
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
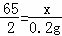 x=6.5g
x=6.5g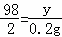 y=9.8g
y=9.8g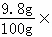 100%=9.8%.
100%=9.8%. 铁,该反应的化学方程式为
铁,该反应的化学方程式为 该反应的化学方程式为
该反应的化学方程式为




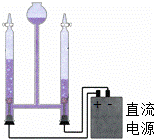
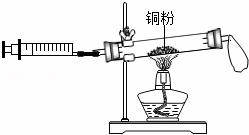
 X↑+2H2O X的化学式为 .
X↑+2H2O X的化学式为 . ( )
( )