题目内容
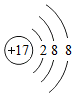
20.如图是电解水的实验图示,给水通以直流电一段时间后的现象如图甲所示,回答下列问题:
(1)A、B分别连接直流电源的两个两极,则A端连接直流电源的负极;验证乙试管内气体的方法是用带火星木条,观察木条是否复燃.
(2)该反应的文字表达式为:水$\stackrel{通电}{→}$氢气+氧气,反应的基本反应类型是分解反应.
(3)实际实验过程中,往往在水中加入少量稀硫酸或氢氧化钠溶液,加入稀硫酸的目的是增强水的导电性.
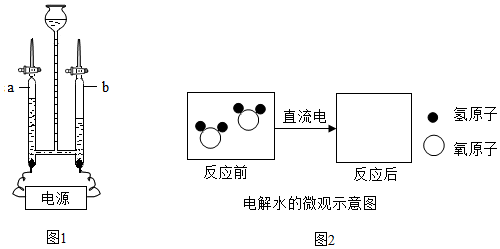
(4)电解水的微观模拟示意图如图乙:
从图中可以看出,宏观上水是由氢、氧(或H、O)元素组成的,微观上每个水分子是由2个氢原子和1个氧原子构成的.
从该模拟图中,你还能获得哪些信息?答出一点即可:化学反应前后原子的种类和数目不变;分子在化学变化中能够再分等.
分析 (1)根据甲试管中气体多,乙试管中气体少,由正氧负氢,氢二氧一,可知A为负极,B为正极,验证氧气用带火星木条,验证氢气用燃着的木条进行解答;
(2)根据水通电分解生成氢气和氧气进行解答;
(3)根据纯水不易导电,在水中加入少量稀硫酸或氢氧化钠溶液,加入稀硫酸的目的增强水的导电性进行解答;
(4)根据分子、原子的在化学变化的变化分析回答有关的问题.
解答 解:(1)甲试管中气体多,乙试管中气体少,由正氧负氢,氢二氧一,可知A为负极,B为正极,甲试管中得到的气体是氢气,乙试管中得到的气体是氧气,验证乙试管内气体的方法是用带火星木条,观察木条是否复燃;
(2)水通电分解生成氢气和氧气,该反应的文字表达式为:水$\stackrel{通电}{→}$氢气+氧气,该反应是一种物质反应生成两种物质,属于分解反应;
(3)纯水不易导电,在水中加入少量稀硫酸或氢氧化钠溶液,加入稀硫酸的目的是增强水的导电性;故填:增强水的导电性;
(4)从宏观上看,水是由氢元素和氧元素组成;从微观上看水是由水分子构成,每个水分子是由2个氢原子和1个氧原子构成的;
从该模拟图中,可以得出分子和原子的概念,分子是保持物质化学性质的一种微粒,原子是化学变化中最小的微粒;
通过上图可以获取的信息:化学反应前后原子的种类和数目不变;分子在化学变化中能够再分等.
答案:
(1)负;用带火星木条,观察木条是否复燃;
(2)水$\stackrel{通电}{→}$氢气+氧气,分解;
(3)增强水的导电性;
(4)氢、氧(或H、O); 2个氢原子和1个氧原子;化学反应前后原子的种类和数目不变;分子在化学变化中能够再分等.
点评 本题考查了电解水的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
10.2008年9月,三鹿婴幼儿奶粉被检出含三聚氰胺,引起全社会的强烈谴责,三聚氰胺的化学式为C3H6N6,根据该化学式你不能获得的信息是( )
| A. | 三聚氰胺是化合物 | |
| B. | 三聚氰胺由碳元素、氢元素和氮元素组成 | |
| C. | 三聚氰胺中碳元素,氢元素和氮元素的质量比为1:2:2 | |
| D. | 一个三聚氰胺分子中有15个原子 |
8.如表是生活中某种常见金属X的部分性质:
(1)试推断金属X可能的一种用途做锅.
(2)将金属X放入硫酸铜溶液中,观察到的现象是金属X表面有红色固体生成.
(3)请自选试剂,设计实验比较金属X与Mg的活动性强弱,完成下表:
| 颜色状态 | 硬度 | 密度 | 熔点 | 导电性 | 导热性 | 延展性 |
| 银白色固体 | 软 | 7.9g/cm3 | 1525℃ | 良好 | 良好 | 良好 |
(2)将金属X放入硫酸铜溶液中,观察到的现象是金属X表面有红色固体生成.
(3)请自选试剂,设计实验比较金属X与Mg的活动性强弱,完成下表:
| 你的一种猜想 | 操作 | 现象 | 结论 |
| 金属X的活动性比镁弱 | 取经打磨的金属X固体,放入氯化镁溶液中 | 无明显现象 | 假设成立,金属X的活动性比镁弱 |
12.在高温下,铁与水蒸气能发生反应生成一种常见的铁的氧化物和一种气体.某兴趣小组请你参与研究:铁与水蒸气反应一段时间后剩余固体物质的成分、性质及再利用.
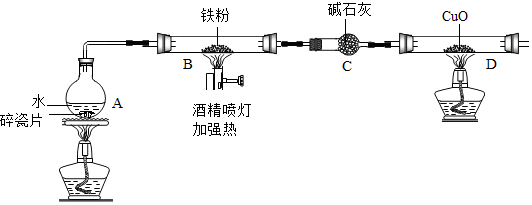
(1)【推断】观察到D中黑色固体变红,则B中生成的气体是氢气.
(2)探究B装置中剩余固体成分是什么?
【查阅资料】
1,碎瓦片能防爆沸,碱石灰是氧化钙和氢氧化钠的混合物
2,铁的氧化物中,只有Fe2O3是红棕色,其余均为黑色,只有Fe3O4能被磁铁吸引.
3,Fe3O4+8HCl═FeCl2+2FeCl3+4H2O
Fe3O4+4H2SO4═FeSO4+Fe2(SO4)3+4H2O
【初步探究】B装置中剩余固体为黑色,能全部被磁铁吸引
【猜想与假设】
猜想一:剩余固体是Fe3O4
猜想二:剩余固体是Fe与Fe3O4
【实验探究】
【实验结论】铁与水蒸气反应的化学方程式为3Fe+4H2O $\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.

(1)【推断】观察到D中黑色固体变红,则B中生成的气体是氢气.
(2)探究B装置中剩余固体成分是什么?
【查阅资料】
1,碎瓦片能防爆沸,碱石灰是氧化钙和氢氧化钠的混合物
2,铁的氧化物中,只有Fe2O3是红棕色,其余均为黑色,只有Fe3O4能被磁铁吸引.
3,Fe3O4+8HCl═FeCl2+2FeCl3+4H2O
Fe3O4+4H2SO4═FeSO4+Fe2(SO4)3+4H2O
【初步探究】B装置中剩余固体为黑色,能全部被磁铁吸引
【猜想与假设】
猜想一:剩余固体是Fe3O4
猜想二:剩余固体是Fe与Fe3O4
【实验探究】
| 实验操作 | 实验现象及结论 |
 .
.
 ”“
”“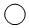 ”画出反应后生成物的微观示意图.
”画出反应后生成物的微观示意图.