题目内容
下表为两种物质在不同温度时的溶解度
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
|
| 溶解度/g | KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
请回答:
(1)60℃时,KCl的溶解度是 g;
(2)40℃时,将30g KCl加入到50g水中,充分溶解后所得溶液是 溶液(填写“饱和”或“不饱和”);
(3)将20℃时KNO3和KCl的两种饱和溶液升温至60℃,则两种溶液的溶质质量分数大小关系是:KNO3 KCl(填写“>”、“<”或“=”).
考点:
固体溶解度的概念;溶质的质量分数、溶解性和溶解度的关系.
专题:
溶液、浊液与溶解度.
分析:
(1)根据表格信息来分析;
(2)根据40℃时,KCl的溶解度来分析;
(3)根据氯化钠、硝酸钾在20℃时的溶解度进行分析.
解答:
解:(1)由表格信息可知,在60℃时,KCl的溶解度是45.5g;故填:45.5;
(2)40℃时,KCl的溶解度为40.0g,也就是在该温度下,100g水中最多溶解40.0g氯化钾就达到饱和状态,那么在该温度下的50g水中最多溶解氯化钾20.0g;故填:饱和;
(3)在20℃时,硝酸钾的溶解度是31.6克,氯化钾的溶解度是34.0克,升高温度后,溶解度变大,所给溶质质量不变,溶液质量不变,所得溶液中溶质的质量分数还是20℃时,氯化钾、硝酸钾的溶质质量分数,在20℃时,KNO3饱和溶液的溶质质量分数小于KCl的饱和溶液的溶质质量分数,所以将20℃时KNO3和KCl的饱和溶液同时升高一定温度后,所得溶液中溶质的质量分数的大小关系是:硝酸钾<氯化钾.故填:<.
点评:
在解此类题时,首先分析题中所给物质溶解度受温度影响的关系,然后结合学过的知识对题中的问题进行解答.

 优化作业上海科技文献出版社系列答案
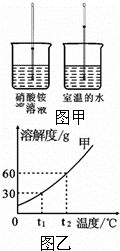
优化作业上海科技文献出版社系列答案KNO3与NH4Cl的溶解度曲线如图所示,下列说法错误的是( )

|
| A. | 常温下,NH4Cl易溶于水 |
|
| B. | t2℃,两种溶液中溶质的质量分数一定相等 |
|
| C. | t3℃,KNO3的溶解度大于NH4Cl的溶解度 |
|
| D. | 两种饱和溶液从t2℃降到t1℃时,均有晶体析出 |
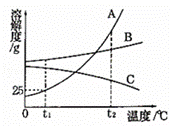
甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示.下列说法正确的是( )
|
| A. | 甲物质的溶解度大于乙物质的溶解度 |
|
| B. | t1℃时,甲、乙两种物质各50g分别加入到100g水中,充分溶解,得到的溶液质量都是140g |
|
| C. | t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数 |
|
| D. | t2℃时甲、乙的饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙 |
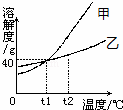
如图是甲、乙两种物质的溶解度曲线,下列说法正确的是( )

|
| A. | 甲的溶解度大于乙的溶解度 |
|
| B. | t1℃时等质量甲、乙两种物质的饱和溶液中溶质质量相等 |
|
| C. | t2℃时等质量甲、乙两种物质的饱和溶液降温至t1℃时,两溶液中溶质质量分数相等 |
|
| D. | 氧气的溶解度随温度变化的规律与图中的甲相似 |
NaOH、Na2CO3、NaCl在不同溶剂中的溶解度如下表所示.
表1 NaOH、Na2CO3、NaCl分别在水中的溶解度(S/g)
| t/℃ | NaOH | Na2CO3 | NaCl |
| 0 | 42 | 7.1 | 35.7 |
| 10 | 51 | 12.2 | 35.8 |
| 20 | 109 | 21.8 | 36.0 |
| 30 | 119 | 39.7 | 36.3 |
表2 常温下,NaOH、Na2CO3、NaCl分别在乙醇中的溶解度(S/g)
| NaOH | Na2CO3 | NaCl |
| 17.3 | <0.01 | 0.1 |
根据表1和表2提供的数据回答下列问题:
(1)NaOH在水中的溶解度随温度升高而 (填“增大”或“减小”)
(2)20℃时,饱和食盐水中溶质的质量分数为 (计算结果精确到0.1%);
(3)为证明CO2能与NaOH发生反应,小明同学将CO2通入饱和NaOH的乙醇溶液中.请推测该实验可观察到的现象 ,推测依据是 .
2014年4月,兰州市局部自来水中苯(C6H6)含量严重超标,引发市民恐慌,苯的沸点为80.1℃,熔点为5.5℃,难溶于水,有剧毒,下列有关苯的说法中正确的是()
|
| A. | 苯属于有机物 |
|
| B. | 苯是由6个碳原子和6个氢原子构成的 |
|
| C. | 常温下可通过滤纸过滤的方法除去水中的苯 |
|
| D. | 可通过加热蒸发的方法除去水中的苯 |