题目内容
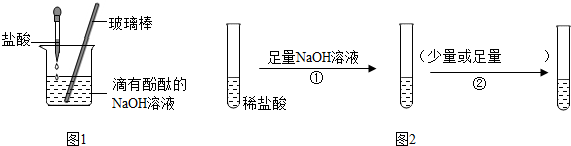
9.氢氧化钠溶液与稀盐酸发生中和反应时观察不到明显现象,为了确定其反应是否发生,某班同学设计了不同的实验方案进行探究.(1)按照如图1的方式,向烧杯中逐滴滴入盐酸至过量的过程中,能够说明盐酸与氢氧化钠发生了化学反应的实验现象是溶液由红色变为无色;
(2)按照如图2的方案完成实验:其中②处不可以选择的试剂是B(填序号,下同),若①②颠倒顺序,仍能证明盐酸与氢氧化钠发生了反应,这种试剂是C;
A.Zn粒 B.AgNO3溶液 C.石蕊试液 D.Na2CO3溶液
(3)下列方案中,能证明氢氧化钠溶液与稀盐酸发生了反应的是AB(填序号);
A.用pH试纸测定氢氧化钠溶液的pH值,然后向其中滴加稀盐酸,pH逐渐减少,最终小于7
B.用温度计测试氢氧化钠溶液滴加稀盐酸前后的温度,温度明显上升
C.向一定的氢氧化钠溶液中滴加硫酸铜溶液,有蓝色沉淀生成,再加稀盐酸后沉淀消失
分析 (1)根据指示剂的变色反应分析;
(2)根据氢离子的验证方法分析;
(3)A、测量反应后的酸碱性与原溶液的酸碱性比较分析,
B、根据化学反应会产生能量,使溶液的温度改变等原因进行分析,
C、沉淀消失只说明盐酸与沉淀反应.
解答 解:(1)氢氧化钠呈碱性,能使无色酚酞试液变红,加入盐酸的过程中要不断搅拌,使盐酸与氢氧化钠充分反应,防止局部酸液过量,酚酞在中性或酸性溶液中都显无色,当红色消失时说明盐酸与氢氧化钠发生了反应;
(2)盐酸和氢氧化钠发生反应的方程式为:HCl+NaOH═NaCl+H2O;由于加入足量的氢氧化钠溶液,所以如果发生反应,溶液显碱性,可以用Zn粒、石蕊试液、Na2CO3溶液验证溶液中是否有氢离子;但是AgNO3溶液与NaCl同样会生成沉淀,无法验证HCl是否参加了反应,若①②颠倒顺序,加入石蕊试液后溶液会从红色变为紫色再变为蓝色,仍能证明盐酸与氢氧化钠发生了反应.
(3)A、氢氧化钠的PH值大于7,滴入盐酸后,溶液PH值逐渐减小,最终小于7说明两者发生了化学反应,故A正确,
B、氢氧化钠与盐酸的反应属于放热反应,依据温度的变化可以判断发生了化学反应,故故B正确,
C、沉淀消失只说明盐酸与沉淀反应,不能说明氢氧化钠溶液与稀盐酸发生了反应,故C错误,
故选:A、B
故答案为:(1)溶液由红色变为无色,(2)B;C;(3)AB
点评 本题主要考查了利用反应现象和能量变化来分析中和反应是否发生,综合性较强.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
17.我国已实施“嫦娥工程”探月计划,人类探月的重要目的之一是勘察、获取地球上蕴藏量很小而月球上却极为丰富的核聚变燃料“He-3”,以解决地球能源危机.已知“C-13”是指原子核内含有6个质子、7个中子的碳原子,则“He-3”所指的氦原子核内( )
| A. | 含有3个质子,没有中子 | B. | 含有2个质子,1个中子 | ||
| C. | 含有1个质子,2个中子 | D. | 含有3个中子,没有质子 |
4.丙烷(C3H8)通常用来作为打火机的燃料,下列有关丙烷的说法不正确的是( )
| A. | 从分类上看:属于有机化合物 | |
| B. | 从构成上看:由3个碳原子和8个氢原子构成 | |
| C. | 从组成上看:由碳、氢两种元素组成 | |
| D. | 从变化上看:完全燃烧会生成二氧化碳和水 |
18.下列各组物质按单质、有机物、混合物顺序排列的是( )
| A. | 生铁、碳酸钙、矿泉水 | B. | 氢气、乙醇、石油 | ||
| C. | 氨气、葡萄糖、冰水共存物 | D. | 红磷、一氧化碳、空气 |
19.染发时常用到的着色剂──对苯二胺,化学式为C6H8N2,是一种有毒化学药品,有致癌性.下列说法正确的是( )
| A. | 对苯二胺中含有N2分子 | |
| B. | 对苯二胺是有机高分子化合物 | |
| C. | 对苯二胺分子中碳原子、氢原子和氮原子个数比为3:4:1 | |
| D. | 对苯二胺中氢元素的质量分数最大 |